مبانی شیمی
نویسنده:
مبانی شیمی
مولکول کوچکترین ذره از یک ماده است که تمام خواص آن ماده را دارا می باشد.ترکیب به ماده ای گفته می شود که مولکول های آن از چند نوع اتم تشکیل شده است.
نیروهایی که اتم های یک مولکول را به هم متصل می کنند، پیوند شیمیایی نام دارند.
شیمی یک زبان جهانی دارد که در آن:
•
حرف ها، نماد های شیمیایی
• کلمات، فرمول های شیمیایی
• جملات، معادلات شیمیایی
هستند
• کلمات، فرمول های شیمیایی
• جملات، معادلات شیمیایی
هستند
واکنش شیمیایی چیست؟
واکنش یک فرآیند شیمیایی است که منجر به شکستن پیوندهای شیمیایی و تشکیل پیوندهای جدید می باشد.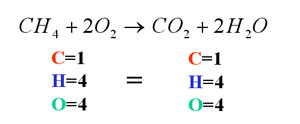
واکنش شیمیایی سوختن متان
برای برقراری برابری تعداد کل اتم های هر عنصر در دو طرف واکنش عمل موازنه انجام می شود.
الکترون، نوترون و پروتون ذرات تشکیل دهنده اتم می باشند.
نیرویی که اتم ها را در یک مولکول به هم متصل می کند، پیوند نام دارد.
والانس یا ظرفیت به تعداد پیوندهایی می گویند که یک اتم می تواند تشکیل دهد.
پیوندی که در آن پخش بار الکتریکی متقارن نباشد را پیوند قطبی می گویند. در یک پیوند قطبی در سر منفی تجمع الکترون و در سر مثبت کمبود الکترون وجود دارد. پیوند قطبی را با یک فلش نمایش می دهند. این فلش یا پیکان از سر مثبت به سمت منفی رسم می شود. زیرا پیوند از جنس نیرو است و نیرو یک کمیت برداری می باشد. مولکولی که یک سر مثبت و یک سر منفی داشته باشد را مولکول قطبی می نامند. مولکول آب نمونه ای از یک مولکول قطبی می باشد.
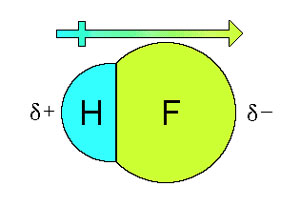
پیوند قطبی
برای درک پدیده قطبی بودن مولکول آب آزمایش شانه پلاستیکی می تواند مفید باشد. شانه پلاستیکی در اثر مالش به لباس الکترون های خود را از دست می دهد و بار مثبت پیدا می کند. به همین علت وقتی نزدیک جریان آب قرار داده می شود مولکول های آب را از سر منفی جذب می کند.

یون چیست؟
اتم وقتی الکترون از دست می دهد به یون مثبت یا کاتیون تبدیل می شود.
اتم وقتی الکترون جذب می کند به یون منفی یا آنیون تبدیل می شود.
کاتیون ها و آنیون ها نسبت به یکدیگر جاذبه دارند. پیوند یونی مولکول NaCl نمونه ای از یک پیوند یونی است.
مجموع بار الکتریکی مثبت و منفی در یک مولکول یکسان است. به این اصل، اصل خنثایی الکتریکی گفته می شود.
پیوند یونی بسیار قوی است. به طوری که برای گسستن آن از طریق حرارت، انرژی بسیار زیادی لازم است. ولی همین پیوندهای یونی از طریق انحلال به راحتی جدا می شوند. مثلاً نمک در آب به خوبی حل می شود.
حلالیت چیست؟
حلالیت یا انحلال پذیری به بیشترین مقدار ماده ای که در یک دمای معین می تواند در حجم معینی از یک حلال حل شود، گفته می شود.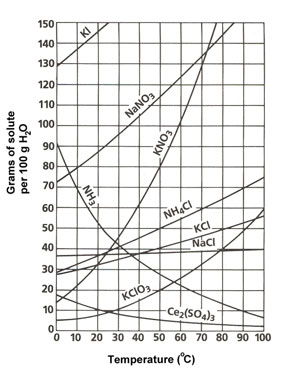
شکل: منحنی انحلال پذیری مواد مختلف در آب
انحلال مواد جامد در آب فقط با دما ارتباط مستقیم دارد.
حداقل اکسیژن محلول در آب که مورد نیاز جانور آبزی می باشد را DO می گویند. برخی ماهی ها به DO بالاتری نیاز دارند. s
اتمسفر چیست؟
پوشش نازکی از هوای اطراف زمین که ما در آن زندگی می کنیم را هواکره یا اتمسفر می گویند.آلوده شدن هوا با کشف آتش آغاز گردید.
هواکره و آب کره
هواکره نام دیگر اتمسفر و آب کره نام دیگر اقیانوس ها است.
•
در هواکره هرچه بالاتر رویم، فشار کاهش می یابد.
• در آب کره هرچه پایین تر رویم، فشار افزایش می یابد.
• در آب کره هرچه پایین تر رویم، فشار افزایش می یابد.
مفهوم فشار
فشار نیروییست که بر واحد سطح وارد می گردد.فشار هوا، فشاریست که از طرف هواکره به اجسام وارد می شود. از آنجا که فشار هوا در همه جهات به درون و بیرون بدن ما وارد می شود، بدن ما فشار هواکره را احساس نمی کند.
برای اندازه گیری فشار از دستگاه هایی مثل بارومتر و مانومتر استفاده می شود.
•
بارومتر جهت اندازه گیری فشار هوا استفاده می شود.
• مانومتر برای اندازه گیری فشار گاز محبوس در یک ظرف سربسته استفاده می شود.
قانون بویل
در دمای ثابت حاصل ضرب فشار در حجم یک گاز مقدار ثابتی است.
• مانومتر برای اندازه گیری فشار گاز محبوس در یک ظرف سربسته استفاده می شود.
قانون شارل در فشار ثابت حجم گاز با دمای گاز نسبت مستقیم دارد.

gas-laws-2.jpg
قوانین گازها: قانون بویل، قانون چارلز و قانون آووگادرو در شکل نشان داده شده است.

gas-laws.jpg
طبق قانون چارلز در فشار ثابت حجم با دما متناسب است به عبارت دیگر هرچه دمای گاز افزایش مییابد حجم گاز افزایش می یابد قانون بویل می گوید در دمای ثابت هرچه فشار یک گاز افزایش پیدا می کند حجم گاز کمتر می شود. قانون آووگادرو میگوید در فشار و دمای ثابت، هرچه تعداد مول های گاز افزایش می یابد حجم گاز افزایش می یابد. ترکیب قوانین چارلز، بویل و آووگادرو میگویند: حجم با نسبت دما به فشار متناسب است.
صفر مطلق چیست؟
صفر مطلق از برون یابی ترسیمه حجم بر حسب دما به دست می آید.مقیاس کلوین، مقیاسی برای اندازه گیری درجه حرارت با در نظر گرفتن صفر مطلق به عنوان مبنا می باشد.

صفر مطلق از برون یابی ترسیمه حجم بر حسب دما به دست می آید.
گاز ایده آل چیست؟
گازی که مطابق نظریه جنبشی گازها رفتار کند را گاز ایده آل می نامند. مطابق این نظریه:1- حجم ذرات گاز بسیار کوچک است.
2- فشار گاز نتیجه برخورد ذرات به دیواره است.
3- مقدار کل انرژی جنبشی ثابت است.
4- میانگین انرژی جنبشی همه گازها ثابت و با هم برابر است.

ideal-gas-law.jpg
قانون گازهای ایده آل حاصلضرب فشار در حجم برابر است با حاصلضرب تعداد مول های گاز در ثابت نسبیت در دما بر حسب کلوین
اکسایش و احتراق
اکسیداسیون یا اکسایش به مفهوم اکسیده شدن، حاصل واکنش اکسیژن با عناصر دیگر است.اکسید به ترکیبی گفته می شود که از واکنش اکسیژن با عناصر دیگر به وجود می آید.
احتراق یا سوختن به اکسیداسیون بسیار سریع همراه با آزاد شدن گرما، نور و صدا گفته می شود. زنگ زدن، اکسیداسیون ملایم است. موازنه به معنای برابری تعداد اتم ها در آغاز و پایان واکنش شیمیایی است.
به عبارت دیگر تعداد هر اتم در طرف اول معادله شیمیایی باید با طرف دوم برابر باشد.
مول یک واحد شمارش است و به تعداد 6.022 × 1023 عدد از هر چیز گفته می شود.
تعداد اتم ها و مولکول ها را با واحد مول بیان می کنند.
جرم یک مول از هر چیز را جرم مولی می گویند.
جرم اتمی به جرم یک مول اتم گفته می شود.
جرم مولکولی، به جرم یک مول مولکول گفته می شود.
عناصر بر اساس شباهت ها و تفاوت های آن ها، طبقه بندی می شوند.
در جدول تناوبی عناصر، عنصرها به سه دسته فلز، شبه فلز و نافلز طبقه بندی شده و عناصر هر طبقه در کنار یکدیگر قرار گرفته اند.
•
قانون پایستگی ماده: تعداد کل اتم های موجود در کره زمین ثابت است ولی طرز قرار گرفتن آن ها در کنار هم در واکنش های شیمیایی تغییر می کند.
• قاون پایستگی جرم: جرم نه به وجود می آید و نه از بین می رود. در یک واکنش شیمیایی مجموع جرم واکنش دهنده ها با مجموع جرم محصولات یکسان است.
• قاون پایستگی جرم: جرم نه به وجود می آید و نه از بین می رود. در یک واکنش شیمیایی مجموع جرم واکنش دهنده ها با مجموع جرم محصولات یکسان است.
هیدروکربن چیست؟
هیدروکربن ها شاخه ای از ترکیبات آلی هستند که از هیدروژن و کربن تشکیل شده اند. هیدروکربن هایی که در آن هر اتم کربن با 4 اتم دیگر پیوند دارد را هیدروکربن سیرشده می نامند.هیدروکربن هایی که در ساختار مولکولیشان اتم هایی از کربن وجود دارد که با پیوندهای دوگانه و سه گانه با اتم های دیگر در ارتباطند را هیدروکربن های سیر نشده می نامند.
آلکان ها و سیکلوآلکان ها، سیر شده اند.
آلکن ها و آلکین ها و ترکیبات آروماتیک، سیر نشده اند.
هرچه آلکان بزرگتر باشد، تعداد اتم کربن بیشتری داشته و نقطه جوش بالاتری خواهد داشت.
برای تبدیل مولکول های کم مصرف به مولکول های پر مصرف از فرآیند تبدیل مولکول ها استفاده می شود.
کراکینگ، پلیمریزاسیون و آلکیلاسیون از مهمترین فرآیندهای تبدیل هستند.
کراکینگ، شکستن مولکول های بزرگ به کوچک است. کراکینگ دو نوع گرمایی و کاتالیزوری دارد.
پلیمریزاسیون یا بسپارش به فرآیند تبدیل مولکول های کوچک به پلیمر گفته می شود.
پتروشیمی دانش تبدیل فرآورده های نفتی به فرآورده های غیرنفتی است.
اتیلن، متان و پروپیلن جزء فرآورده های نفتی محسوب می شوند.
لاستیک، پارچه، حشره کش و دارو جزء فرآورده های غیرنفتی محسوب گردیده و مواد پتروشیمیایی یا فرآورده های پتروشیمی نامیده می شوند.
پلیمرها در واقع فرآورده های پتروشیمی هستند.
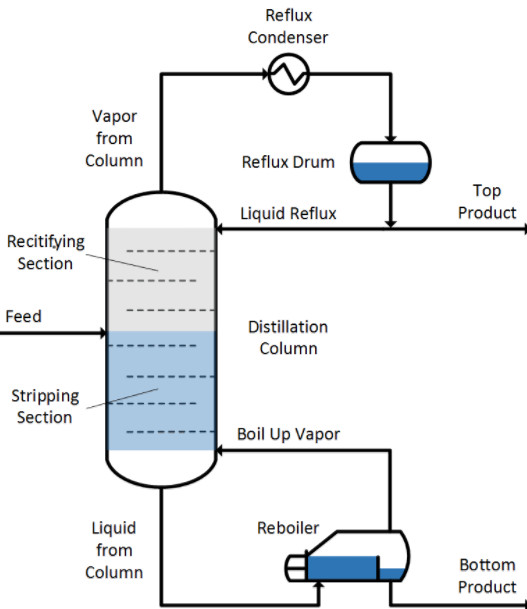
A-fractionating-column-is-an-essential-item-used-in-distillation-of-liquid-mixtures-so-as-to-separate-the-mixture-into-its-component-parts,-or-fractions,-based-on-the-differences-in-volatilities.jpg
ستون تقطیر یا جداسازی برای تقطیر مخلوط های مایع استفاده میشود و یک آمیزه ی مایع را به اجزای تشکیل دهنده اش (برش هایش) بر اساس فراریت، جداسازی می کند.

fractional-distillation.jpg
ستون تقطیر نفت خام در این شکل نمایش داده شده است: همانطور که می بینید برشهای ۷۰ کربن و بالاتر برای ساخت آسفالت استفاده می شود. برش های ۲۰ و ۷۰ کربنه برای ساخت سوخت کشتی ها و بویلر ها استفاده می شود. برش های ۲۰ تا ۵۰ کربن برای ساخت روغن های روان کننده، موم ها و جلا دهنده ها استفاده میشود. برش ۱۴ تا ۲۰ کربن برای سوخت کامیون و ماشینهای سنگین است. برش ۱۰ تا ۱۶ کربن همان نفت سفید است که برای سوخت هواپیما یا برای تولید حرارت استفاده می شود. برش ۵ تا ۱۰ کربن به عنوان بنزین در اتومبیل استفاده می شود. برش های ۱ تا ۹ کربن را در صنعت پتروشیمی استفاده می کنند. بالاترین برش ستون تقطیر نفت خام، هیدروکربن های یک تا چهار کربنه است که گازی هستند و مصرف سوخت گاز مواد اولیه پتروشیمی و سوخت ماشین های گازسوز یا LPG استفاده می شود.
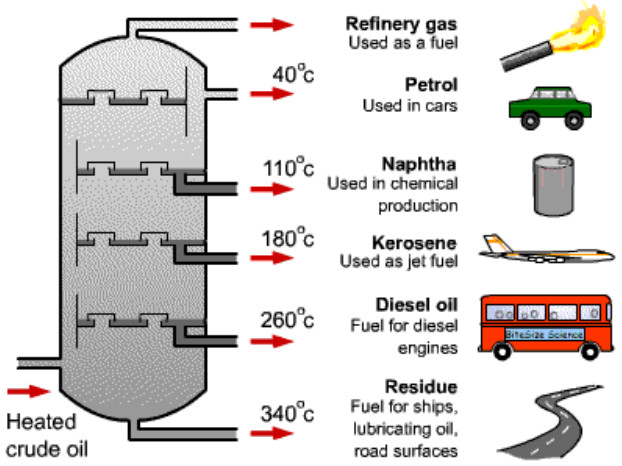
fractions-of-distillation-column-2.jpg
در ستون تقطیر نفت خام از سینی های مختلف در دماهای مختلف برش های متفاوتی ایجاد می شود. مثلاً در دمای ۴۰ درجه، سوخت اتومبیل. در دمای ۱۱۰ درجه، نفتا برای تولید مواد شیمیایی. در دمای ۱۸۰ درجه کروسین یا نفت سفید برای هواپیما. در دمای ۲۶۰ درجه، روغن دیزل یا سوخت دیزل اتوبوس ها و کامیون ها. در دمای ۳۴۰ درجه سوخت کشتی ها، روان کننده و آسفالت.
تبخیر سطحی چیست؟
اگر این مولکول های یک مایع در اثر برخورد به سطح تماس مایع و هوا بر نیروی کششی سطحی غلبه کرده و به فاز هوا وارد شوند، تبخیر سطحی اتفاق می افتد. نکته: هرچه دما بیشتر باشد، تعداد این برخوردها زیادتر شده و شدت تبخیر سطحی بیشتر می شود.انرژی یونش یا انرژی یونیزاسیون
انرژی لازم برای جدا کردن سست ترین الکترون از اتم گازی و تبدیل آن به یون مثبت گازی را انرژی یونیزاسیون نخست می گویند. واحد انرژی یونیزاسیونE1 ، کیلوژول بر مول KJ/mol است.با مطالعه انرژی های یونش و مشاهده جهش های بزرگ و کوچک می توان لایه های اصلی و فرعی الکترونی را تعیین نمود.
•
جهش های بزرگ نشان دهنده تغییر در لایه های اصلی است.
• جهش های کوچک نشان دهنده تغییر لایه های فرعی است.
با مطالعه انرژی یونش عناصر مختلف و رسم نمودار E1 بر حسب N می توان گروه های اتمی را تعیین نمود.
• جهش های کوچک نشان دهنده تغییر لایه های فرعی است.
لایه های الکترونی یا ترازهای انرژی به ترتیب از پایین ترین سطح انرژی به وسیله الکترون ها اشغال می شوند.
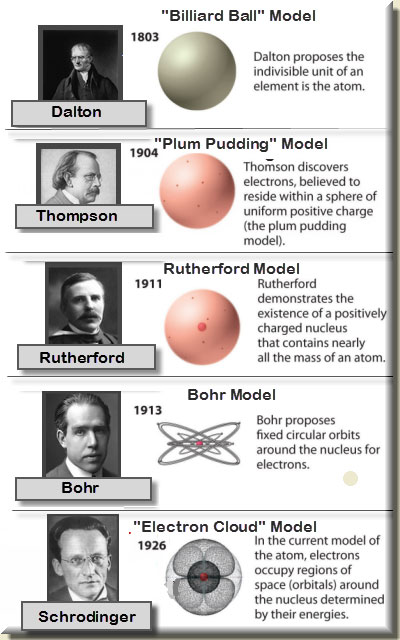
مدل اتمی چیست؟
برای پاسخ به این سوال، اول باید بگوییم مدل چیست؟مدل چیست؟
مدل توصیفی برای اجسامیست که نمی توانیم آن ها را مشاهده کنیم.معمولاً برای اجسام خیلی بزرگ یا خیلی کوچک از مدل استفاده می شود.
مدل اتمی بوهر (سیاره ای)، رادرفورد، تامسون و اوربیتالی هر کدام برای توصیف اتم ها استفاده می شوند.
گرچه نظریه برخی از این مدلها رد شده است، اماهیچ کدام از این مدل ها را کنار نمی گذاریم. بلکه جایی که لازم است، استفاده می کنیم.
مدل ابر الکترونی می گوید هر چه احتمال حضور الکترون بیشتر باشد، تراکم نقاط بیشتر است.
حرکت پرنده حول ظرف دانه، مشابه مدل ابر الکترونی است.
مدل کوانتومی اتم برای توجیه رفتار موجی الکترون ها ارائه شد. مطابق این مدل، حرکت الکترون محدود به یک مسیر دایره ای نیست. بلکه در یک فضای سه بعدی به نام اوربیتال صورت می گیرد.
پرتو کاتدی: به پرتویی که در اثر اختلاف ولتاژ بسیار زیاد بین دو الکترود مثبت و منفی از الکترود منفی (کاتد) به الکترود مثبت (آند) می تابد، پرتو کاتدی می گویند.
تامسون با مطالعه پرتوی کاتدی نسبت بار به جرم الکترون را اندازه گرفت.
میلیکان بار الکتریکی الکترون را محاسبه نمود.
با ترکیب مطالعه تامسون و میلیکان جرم الکترون به دست آمد.
البته مدل اتمی تامسون زمانی مطرح شد که پروتون هنوز کشف نشده بود و جرم اتم را مربوط به الکترون می دانستند.
کشف مواد پرتوزا (فسفورسانس) باعث کشف هسته اتم گردید.
بعدها از اختلاف عدد جرمی و عدد اتمی، نوترون کشف شد.
عدد اتمی تعداد پروتون های یک اتم است.
عدد جرمی مجموع تعداد پروتون ها و نوترون ها.
اتم های یک عنصر که دارای عدد اتمی یکسان و عدد جرمی متفاوت باشند را ایزوتوپ می گویند.
اوربیتال چیست؟
اوربیتال به فضای اطراف هسته می گویند که احتمال یافتن الکترون در آن بیش از 90 درصد می باشد.اوربیتال های S به شکل کره و اوربیتال های P به شکل دمبل می باشند.
ترتیب پر شدن اوربیتال ها از پایین ترین سطح انرژی به بالاترین سطح انرژی است.
در هر اوربیتال، حداکثر دو الکترون با اسپین مخالف می تواند قرار گیرد (اسپین به جهت چرخش یک الکترون به دور خود می گویند).
اصل طرد پاولی: هیچ اوربیتالی در یک اتم نمی تواند بیش از دو الکترون در خود جای دهد.
اصل هوند: در اوربیتال های هم انرژی، جفت شدن هنگامی صورت می گیرد که همه اوربیتال های هم انرژی نیمه پر با اسپین یکسان باشند.
بنابراین در اصل هوند، هم انرژی بودن و هم اسپین بودن، هر دو شرط اصلی هستند.
چگونه دو الکترون در یک اربیتال قرار می گیرند؟ دو الکترون در یک اوربیتال در اثر همنام بودن بار الکتریکی از هم دفع می شوند و به علت مخالف بودن اسپینشان به هم جذب می شوند. بین این دافعه الکترواستاتیکی و جاذبه مغناطیسی تعادل برقرار است.
انواع پیوندهای شیمیایی
پیوند یونی در اثر جاذبه الکترواستاتیک بین یون های ناهمنام به وجود می آید. عامل ایجاد پیوند یونی، انتقال الکترون است.پیوند کووالانسی در اثر موازنه:
نیروهای جاذبه هسته –الکترون
و
دافعه هسته هسته و الکترون الکترون
به وجود می آید.
و
دافعه هسته هسته و الکترون الکترون
عامل ایجاد پیوند کووالانسی اشتراک الکترون است.
اختلاف الکترونگاتیوی باعث ایجاد قطبیت در پیوند کووالانسی می شود.
پیوندهای مولکولی به دو دسته کپسایسینوالسی و هیدروژنی تقسیم بندی می شوند.
پیوندهای واندروالسی دو نوع هستند:
دوقطبی – دوقطبی: نیروی بین دو مولکول قطبی دائم
لاندن: نیروی دو مولکول با قطبیت لحظه ای
در پیوندهای هیدروژنی، هیدروژن به صورت پلی بین دو اتم الکترونگاتیو قرار می گیرد.
لاندن: نیروی دو مولکول با قطبیت لحظه ای
الکترونگاتیوی تمایل و توانایی یک اتم برای کشیدن جفت الکترون پیوندی به سمت هسته خود می باشد.
پیوند داتیو، پیوند کووالانسی بین دو اتمی است که یکی دهنده و دیگری پذیرنده جفت الکترونی می باشد.
پیوند فلزی شبکه سه بعدی از ذرات مثبت است که در دریایی از الکترون ها مستقر می باشد. در پیوند فلزی، ذرات مثبت مستقر و الکترون های ظرفیت غیرمستقر هستند. الکترون های غیرمستقر همانند چسبی ذرات مثبت را از طریق نیروهای جاذبه الکترواستاتیک به یکدیگر متصل نگه می دارند.
اگر پیوندهای قطبی در یک مولکول طوری قرار گیرند که راستایشان یکسان ولی دقیقاً در جهت مخالف هم باشند، مولکول ایجاد شده غیرقطبی خواهد بود.
شعاع واندروالسی به نصف فاصله هسته های دو اتم مجاور گفته می شود.
انرژی گرمایی به مجموع انرژی جنبشی یک ماده گفته می شود.
انرژی شیمیایی، انرژی ذخیره شده در مولکول های یک ماده است.
به موادی که در اثر واکنش های شیمیایی انرژی گرمایی زیادی آزاد می کنند، مواد پرانرژی می گویند.
انرژی درونی به مجموعه انرژی جنبشی و پتانسیل یک ماده می گویند و آن را با حرف E نمایش می دهند.
آنتالپی به مجموع انرژی درونی و حاصل ضرب فشار در حجم می گویند و آن را با حرف H نمایش می دهند.

رابطه آنتالپی و انرژی درونی
H = E + PV
گرمای سوختن: گرمای حاصل از انجام یک واکنش سوختن را گرمای سوختن می گویند.
انرژی لازم برای شکستن یک پیوند را انرژی پیوندی می گویند.
هرچه تعداد مولکول های حاصل از واکنش بیشتر شود، بی نظمی افزایش می یابد.
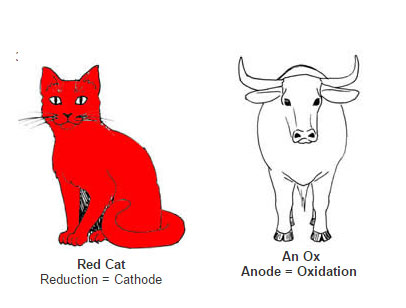
واکنش های اکسایشی کاهشی
واکنشی را که در آن انتقال الکترون اتفاق می افتد، واکنش اکسایشی کاهشی می گویند.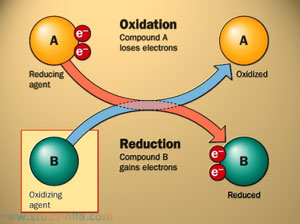
کاهش به معنای به دست آوردن الکترون است. (کاهش = احیا)
آهن خالص خیلی دیر زنگ می زند. ناخالصی ها باعث افزایش سرعت زنگ زدن آهن می شوند.
آهن گالوانیزه از فرو بردن آهن در روی مذاب تهیه می شود. روی و آهن دو الکترود پیل الکتروشیمیایی موجود در آهن گالوانیزه را تشکیل می دهند. قطعه های فلز روی به تدریج الکترون داده و خورده می شوند. این الکترون ها به عنوان طعمه توسط اکسیژن محیط مصرف شده و از اکسید شدن آهن جلوگیری می کنند.
جدول تناوبی
قانون تناوبی: هرگاه عنصرها بر حسب افزایش عدد اتمی در کنار یکدیگر قرار دهیم، خواص فیزیکی و شیمیایی آن ها به صورت تناوبی تکرار می شود. به این قانون، قانون تناوبی عناصر می گویند.ویژگی های گروهی عناصر
مطابق جدول تناوبی، عناصر موجود در طبیعت به 4 دسته فلز، شبه فلز، غیرفلز و گاز نجیب تقسیم بندی می شوند.80 درصد عناصر جدول تناوبی، فلز هستند.
فلزات به 3 گروه قلیایی، قلیایی خاکی و واسطه تقسیم بندی می شوند.
The-periodic-table-.jpg
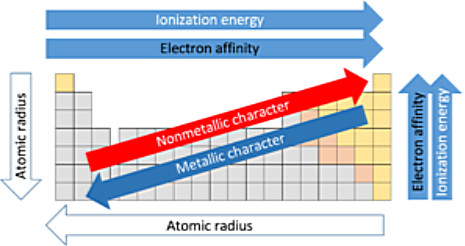
در جدول تناوبی هر چه به سمت راست میرویم انرژی یونیزه شدن افزایش پیدا میکند و تمایل به الکترون افزایش پیدا میکند. در گروهها هرچه به پایین میرویم، شعاع اتمی افزایش مییابد. عناصر سمت چپ جدول تناوبی شعاع اتمی پایینتری دارند. عناصر بالای جدول تناوبی تمایل بیشتری به الکترون دارد و انرژی یونش آنها بیشتر است. هر چه به سمت بخش راست بالای جدول میرویم خاصیت غیرفلزی افزایش پیدا میکند و هرچه به سمت چپ پایین جدول میرویم خاصیت فلزی افزایش پیدا میکند.
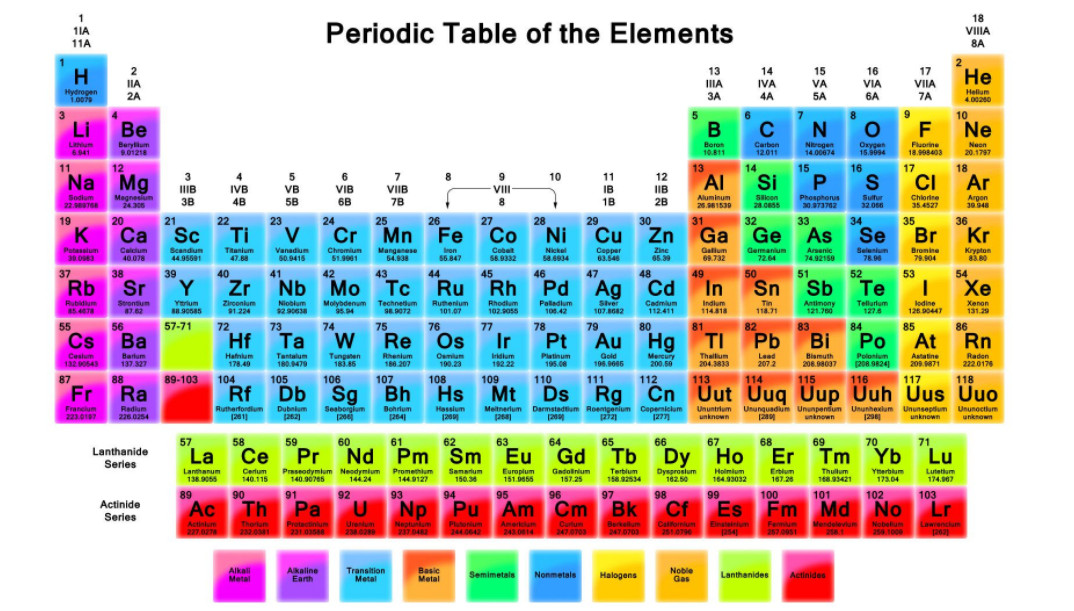
The-periodic-table-is-a-tabular-arrangement-of-the-chemical-elements,-ordered-by-their-atomic-number,-electron-configurations,-and-recurring-chemical-properties.jpg
جدول تناوبی یک آرایش جدولی برای عناصر شیمیایی است که به ترتیب عدد اتمی، شکل الکترونی و خواص شیمیایی طبقهبندیشده است.
رسیدن به آرایش هشت تایی از دو طریق امکان پذیر است:
1- انتقال الکترون و تشکیل پیوندهای یونی: وقتی اختلاف الکترونگاتیوی بالا باشد.
2- اشتراک الکترون و تشکیل پیوندهای کووالانسی: وقتی اختلاف الکترونگاتیوی پایین باشد.
2- اشتراک الکترون و تشکیل پیوندهای کووالانسی: وقتی اختلاف الکترونگاتیوی پایین باشد.

The-octet-rule-is-a-chemical-rule-of-thumb-that-reflects-observation-that-atoms-of-main-group-elements-tend-to-combine-in-such-a-way-that-each-atom-has-eight-electrons-in-its-valence-shell.jpg
قانون اُکتِت: یک قانون شیمیایی است که می گوید اتمهای گروه اصلی عناصر تمایل دارند بهگونهای آمیخته شوند که هر اتم، هشت الکترون در لایه ظرفیت وجود داشته باشد.

The-octet-rule.jpg
قانون اکتت میگوید اتمها تمایل دارد الکترونهایشان را از دست بدهد یا الکترون به دست آورند یا الکترون به اشتراک بگذارند تا با هشت الکترون لایه ظرفیت (4 جفت الکترون) احاطه شوند.
کربن عنصر تشکیل دهنده جهان زنده است.
سیلیس عنصر تشکیل دهنده جهان غیرزنده می باشد.
شیمی آلی به بررسی ترکیبات کربن و خواص آن ها گفته می شود.
در جدول تناوبی عناصر، کربن بین فلزات و نافلزات قرار دارد. نه تمایل الکترون از دست بدهد، نه تمایل دارد الکترون بگیرد. در عوض هر چهار الکترون لایه ظرفیت خود را به اشتراک می گذارد.
الماس و گرافیت دگرشکل های مختلف کربن هستند. (دگرشکل = آلوتروپ)
گروه عاملی به آرایش ویژه ای از اتم ها گفته می شود که مولکول آلی حاوی آن دارای خواص فیزیکی و شیمیایی منحصر به فردی می شود.
•
• مبانی شیمی

برای اطلاع از سرفصل های پکیج آموزشی، کلمه اسکین تراپی را با واتسپ به شماره 09101971690 بفرستید یا روی لینک اسکین تراپی کلیک کنید و اینترنتی خرید کنید
معادل انگلیسی اصطلاحات تخصصی این مطلب
2- قلیا = Alkali قلیا، باز متضاد اسید
قلیاها، مواد قلیایی، بازها، مواد با خاصیت بازی
عصب هایی که پیام را از حسگرهای بیرونی دریافت نموده و به مغز منتقل می کنند.
alkalinity = قلیاییت
alkalizing agent = عامل قلیایی کننده، ماده ای که به محصول خاصیت قلیایی می دهد، مثل آمونیاک در رنگ مو
alkalizing ingredient = ماده قلیایی کننده
desincrustation or an alkaline softening solution = دزن یا محلول نرم کننده قلیایی
قلیاها، مواد قلیایی، بازها، مواد با خاصیت بازی
عصب هایی که پیام را از حسگرهای بیرونی دریافت نموده و به مغز منتقل می کنند.
alkalinity = قلیاییت
alkalizing agent = عامل قلیایی کننده، ماده ای که به محصول خاصیت قلیایی می دهد، مثل آمونیاک در رنگ مو
alkalizing ingredient = ماده قلیایی کننده
desincrustation or an alkaline softening solution = دزن یا محلول نرم کننده قلیایی
alkalizing ingredient
ماده قلیایی کننده
ماده قلیایی کننده
desincrustation or an alkaline softening solution
دزن یا محلول نرم کننده قلیایی
دزن یا محلول نرم کننده قلیایی
3- شیمی = Chemistry شیمی
organic chemistry = شیمی آلی
AROMA CHEMICALS, Molecules obtained from natural products or made by synthetic organic chemistry that have an aroma. Most of the synthetic aroma chemicals are nature identical, i.e., identical to the same molecule obtained from a natural product. = مواد شیمیایی آروماتیك یا آروماكمیكال ها مولکولهایی هستند كه از محصولات طبیعی به دست میآیند یا به صورت سنتزی ساخته میشوند و بو دارند. بسیاری از مواد شیمایی آروماتیك بوی شبیه مواد طبیعی دارند. به عبارت دیگر شبیه مولکولهایی هستند كه از طبیعت به دست میآیند.
organic chemistry = شیمی آلی
organic chemistry = شیمی آلی
AROMA CHEMICALS, Molecules obtained from natural products or made by synthetic organic chemistry that have an aroma. Most of the synthetic aroma chemicals are nature identical, i.e., identical to the same molecule obtained from a natural product. = مواد شیمیایی آروماتیك یا آروماكمیكال ها مولکولهایی هستند كه از محصولات طبیعی به دست میآیند یا به صورت سنتزی ساخته میشوند و بو دارند. بسیاری از مواد شیمایی آروماتیك بوی شبیه مواد طبیعی دارند. به عبارت دیگر شبیه مولکولهایی هستند كه از طبیعت به دست میآیند.
organic chemistry = شیمی آلی
chemistry
شیمی
شیمی
organic chemistry
شیمی آلی
شیمی آلی
شیمی آلی
شیمی آلی
6- حلال = Solvent حلال
حلال ها
residual solvents = حلال باقیمانده
solvent extraction = استخراج با حلال
EXTRACTION, Extraction with volatile solvents is the most effective and commonly used method to obtain essences. = استخراج: استخراج با حلال های فرّار موثرترین و رایج ترین روش به دست آوردن گیاهان است.
EXTRACTS, Concentrated perfume or flower products obtained through the process of extraction using volatile solvents. = عصاره: محصولات حاصل از استخراج با حلالهای فرّار كه تغلیظ شده است.
ABSOLUTE, Highly concentrated perfume ingredient obtained by the alcohol extraction of the concrete. The concrete is obtained by the solvent extract of the plant material. = ابسولوت به ماده عطری بسیار غلیظ میگویند كه با استخراج الكلی كانكریتها به دست میآید. كانكریت با روش استخراج با حلال از گیاهان به دست میآید.
CONCRETE, Solid waxy substance obtained by the solvent extraction of plant material, e.g., flowers, bark, leaves, etc. The absolute is obtained by alcohol extraction of the concrete. = كانكریت: ماده مومی شكل جامد كه با روش استخراج با حلال از مواد گیاهی مثل گلها، ساقه و برگ درختان به دست می آید. ابسولوت از استخراج الكلی كانكریت ها به دست می آید.
solvent extraction, Liquid–liquid extraction also known as solvent extraction and partitioning, is a method to separate compounds based on their relative solubilities in two different immiscible liquids, usually water and an organic solvent. = استخراج با حلال یا استخراج مایع مایع که به آن پارتیشنینگ نیز می گویند، روشی برای جداسازی ترکیبات بر مبنای حلالیت نسبی آن ها به دو فاز مایع غیر قابل امتزاج (معمولا آب و فاز حلال ارگانیک) می باشد
حلال ها
residual solvents = حلال باقیمانده
solvent extraction = استخراج با حلال
EXTRACTION, Extraction with volatile solvents is the most effective and commonly used method to obtain essences. = استخراج: استخراج با حلال های فرّار موثرترین و رایج ترین روش به دست آوردن گیاهان است.
EXTRACTS, Concentrated perfume or flower products obtained through the process of extraction using volatile solvents. = عصاره: محصولات حاصل از استخراج با حلالهای فرّار كه تغلیظ شده است.
ABSOLUTE, Highly concentrated perfume ingredient obtained by the alcohol extraction of the concrete. The concrete is obtained by the solvent extract of the plant material. = ابسولوت به ماده عطری بسیار غلیظ میگویند كه با استخراج الكلی كانكریتها به دست میآید. كانكریت با روش استخراج با حلال از گیاهان به دست میآید.
CONCRETE, Solid waxy substance obtained by the solvent extraction of plant material, e.g., flowers, bark, leaves, etc. The absolute is obtained by alcohol extraction of the concrete. = كانكریت: ماده مومی شكل جامد كه با روش استخراج با حلال از مواد گیاهی مثل گلها، ساقه و برگ درختان به دست می آید. ابسولوت از استخراج الكلی كانكریت ها به دست می آید.
solvent extraction, Liquid–liquid extraction also known as solvent extraction and partitioning, is a method to separate compounds based on their relative solubilities in two different immiscible liquids, usually water and an organic solvent. = استخراج با حلال یا استخراج مایع مایع که به آن پارتیشنینگ نیز می گویند، روشی برای جداسازی ترکیبات بر مبنای حلالیت نسبی آن ها به دو فاز مایع غیر قابل امتزاج (معمولا آب و فاز حلال ارگانیک) می باشد
solvent extraction
استخراج با حلال
استخراج با حلال
solvent extraction2
solvents
حلال ها
حلال ها
7- آروما = Aroma آروما، ماده معطر، اسانس، ماده خوشبو، ترکیبات آروماتیک
plant aroma = آرومای گیاهی
aromatherapy = آروماتراپی، رایحه درمانی
aromatherapist = آروماتراپیست
عددی برای اندازه گیری میزان محافظت یک فرآورده ضد آفتاب از پوست در برابر پرتوهای آفتاب که به اختصار SPF نامیده می شود.
aromatic agent = ماده معطر و آروماتیک
Chemical aroma = ماده شیمیایی معطر
aroma chemicals = مواد شیمیایی معطر
Aromatic plants = گیاهان معطر
Clove, syzgium aromaticum = میخک، قرنفل، اوژنول
fragrance and aroma ingredients = مواد معطر و خوشبو
Nepalese Cardamom, Amomum aromaticum = هل نپالی
Chinese Cinnamon, Cinnamomum aromaticum = دارچین چینی، سلیخه
AROMA, A term used to describe a sensation which is between smell and taste, such as the aroma of coffee. = آروما، واژهای است كه احساس بین بوییدن و چشیدن را بیان میکند. مثل آرومای قهوه.
ISOLATES, Aroma chemicals that are primarily isolated from natural products. They are highly refined natural substances. = ایزولات ها: مواد شیمیایی كه تركیبات طبیعی جداسازی شدند.
MOSSY, The odor suggestive of the aromatic lichens, and mosses, primarily oak moss and tree moss; reminiscent of forest depths. = خزه ای: بویی كه شبیه مواد معطر لیتن ها، خزه ها مثل خزه بلوط است. یادآور اعماق جنگل.
essential oils, an essential oil is a concentrated hydrophobic liquid containing volatile aroma compounds from plants, also known as volatile oils = اسانس های روغنی، ماده هیدروفوب غلیظ شده که حاوی ترکیبات آروماتیک فرار گیاهان می باشد. اسانس های روغنی را روغن های فرار نیز می نامند.
IONONES, One of the most valued synthetic perfume ingredients. They have a fresh, violet aroma and were first introduced into perfumery in 1936 in Violettes de Toulouse. = آیونونها: یكی از باارزش ترین مواد عطری سنتزی، رایحه تازه و گل بنفشه دارند. در سال 1936 به صنعت عطرسازی معرفی شدند.
FOUGÈRE, The French word for “fern.” Fougère fragrances depend on aromatic chemicals to produce the fern-like notes that combine well with lavender, citrus and coumarin in fragrances for men. = فوژه: لغت فرانسوی فِرن یا سرخس. عطریات فوژه مواد شیمایی آروماتیك برای تولید نوت های سرخس مانند هستند كه از آمیزش لاوندر، سیتروس، كومارین به دست می آید.
AROMA-CHOLOGY, A term coined by The Fragrance Foundation to describe the interrelationship between psychology and the latest in fragrance technology to elicit a variety of specific feelings and emotions. = آروماكولوژی، واژهای كه توسط خانههای عطر ابداع شده تا شرح دهد رابطه بین روانشناسی و تكنولوژی عطر را تا احساسات و عواطف را برانگیزد.
DISTILLATION, A common technique for obtaining aromatic compounds from plants, such as orange blossoms and roses. The raw material is heated and the fragrant compounds are recollected through condensation of the distilled vapour. = تقطیر: تكنیك رایج برای بدست آوردن مواد آروماتیك گیاهان مثل شكوفه پرتقال و رز. ماده اولیه حرارت داده می شود و تركیب عطری جمع آوری می شود با روش میعان مایع تقطیر شده.
AROMA CHEMICALS, Molecules obtained from natural products or made by synthetic organic chemistry that have an aroma. Most of the synthetic aroma chemicals are nature identical, i.e., identical to the same molecule obtained from a natural product. = مواد شیمیایی آروماتیك یا آروماكمیكال ها مولکولهایی هستند كه از محصولات طبیعی به دست میآیند یا به صورت سنتزی ساخته میشوند و بو دارند. بسیاری از مواد شیمایی آروماتیك بوی شبیه مواد طبیعی دارند. به عبارت دیگر شبیه مولکولهایی هستند كه از طبیعت به دست میآیند.
ENFLEURAGE, In this process, aroma materials are absorbed into wax and then the odorous oil is extracted with ethyl alcohol. Extraction by enfleurage was commonly used when distillation was not possible because some fragrant compounds denature through high heat. = انفلوراژ: در این فرایند مواد معطر به داخل یك ماده مومی شكل جذب می شود و سپس روغنهای معطر با اتیل الكل جدا می شود. استخراج با انفلوراژ برای گیاهان ظریف استفاده می شود كه در اثر تقطیر ممكن است ملكولهای مواد معطرشان تخریب شود.
ANIMALIC, Characterized by bodily aromas or aromas most associated with traditional animal materials such as musk, civet and castoreum. These materials are now banned and have been replaced with musks obtained from plants and civet and castoreum smelling molecules obtained synthetically. = انیمالیك یا حیوانی، به بوهایی گفته میشود كه در عطرهای حیوانی سنتی مثل مُشك، سیوت و كاستریوم وجود دارد. این مواد در حال حاضر ممنوع هستند و با مشکهای به دست آمده از گیاهان و مولکولهایی كه بوی شبیه سیوت و كاستریوم میدهند و به صورت سنتزی تشكل شدهاند جایگزین شدهاند.
NEROLI OIL, Neroli essential oil is extracted from the fragrant blossoms of the bitter orange tree and has a beautiful aroma that appeals to men and women alike. In common with rose and jasmine, neroli oil is almost a complete fragrance in itself and forms the heart of one of the worlds most enduring perfumes, ‘Eau de Cologne’. = روغن نرولی: روغنی كه از شكوفه معطر پرتقال تلخ به دست می آید.
AROMATHERAPY, The use of volatile plant oils, including essential oils, for psychological and physical well-being. The therapeutic use of pure essential oils and herbs in body massage,which is described by proponents as “healing, beautifying and soothing” the body and mind.The history of aromatherapy stretches as far back as 6,000 years ago in ancient Egypt. It wasn’t until the 1920’s, however, when the term was actually coined by a French chemist, R.M. Gattefosse. = آروماتراپی، استفاده از روغنهای گیاهی شامل اسانسهای روغنی برای سلامت فیزیكی و فیزیولوژیكی. استفاده درمانی از اسانسهای روغنی خالص و گیاهان در ماساژ بدن، شفابخش، زیباكننده و التیامبخش برای بدن و ذهن میباشد. تاریخچه آروماتراپی به 6 هزار سال پیش به مصر باستان برمیگردد. در سال 1920 این واژه توسط یك شیمیدان فرانسوی به نام گَته فوزه ابداع شد.
plant aroma = آرومای گیاهی
aromatherapy = آروماتراپی، رایحه درمانی
aromatherapist = آروماتراپیست
عددی برای اندازه گیری میزان محافظت یک فرآورده ضد آفتاب از پوست در برابر پرتوهای آفتاب که به اختصار SPF نامیده می شود.
aromatic agent = ماده معطر و آروماتیک
Chemical aroma = ماده شیمیایی معطر
aroma chemicals = مواد شیمیایی معطر
Aromatic plants = گیاهان معطر
Clove, syzgium aromaticum = میخک، قرنفل، اوژنول
fragrance and aroma ingredients = مواد معطر و خوشبو
Nepalese Cardamom, Amomum aromaticum = هل نپالی
Chinese Cinnamon, Cinnamomum aromaticum = دارچین چینی، سلیخه
AROMA, A term used to describe a sensation which is between smell and taste, such as the aroma of coffee. = آروما، واژهای است كه احساس بین بوییدن و چشیدن را بیان میکند. مثل آرومای قهوه.
ISOLATES, Aroma chemicals that are primarily isolated from natural products. They are highly refined natural substances. = ایزولات ها: مواد شیمیایی كه تركیبات طبیعی جداسازی شدند.
MOSSY, The odor suggestive of the aromatic lichens, and mosses, primarily oak moss and tree moss; reminiscent of forest depths. = خزه ای: بویی كه شبیه مواد معطر لیتن ها، خزه ها مثل خزه بلوط است. یادآور اعماق جنگل.
essential oils, an essential oil is a concentrated hydrophobic liquid containing volatile aroma compounds from plants, also known as volatile oils = اسانس های روغنی، ماده هیدروفوب غلیظ شده که حاوی ترکیبات آروماتیک فرار گیاهان می باشد. اسانس های روغنی را روغن های فرار نیز می نامند.
IONONES, One of the most valued synthetic perfume ingredients. They have a fresh, violet aroma and were first introduced into perfumery in 1936 in Violettes de Toulouse. = آیونونها: یكی از باارزش ترین مواد عطری سنتزی، رایحه تازه و گل بنفشه دارند. در سال 1936 به صنعت عطرسازی معرفی شدند.
FOUGÈRE, The French word for “fern.” Fougère fragrances depend on aromatic chemicals to produce the fern-like notes that combine well with lavender, citrus and coumarin in fragrances for men. = فوژه: لغت فرانسوی فِرن یا سرخس. عطریات فوژه مواد شیمایی آروماتیك برای تولید نوت های سرخس مانند هستند كه از آمیزش لاوندر، سیتروس، كومارین به دست می آید.
AROMA-CHOLOGY, A term coined by The Fragrance Foundation to describe the interrelationship between psychology and the latest in fragrance technology to elicit a variety of specific feelings and emotions. = آروماكولوژی، واژهای كه توسط خانههای عطر ابداع شده تا شرح دهد رابطه بین روانشناسی و تكنولوژی عطر را تا احساسات و عواطف را برانگیزد.
DISTILLATION, A common technique for obtaining aromatic compounds from plants, such as orange blossoms and roses. The raw material is heated and the fragrant compounds are recollected through condensation of the distilled vapour. = تقطیر: تكنیك رایج برای بدست آوردن مواد آروماتیك گیاهان مثل شكوفه پرتقال و رز. ماده اولیه حرارت داده می شود و تركیب عطری جمع آوری می شود با روش میعان مایع تقطیر شده.
AROMA CHEMICALS, Molecules obtained from natural products or made by synthetic organic chemistry that have an aroma. Most of the synthetic aroma chemicals are nature identical, i.e., identical to the same molecule obtained from a natural product. = مواد شیمیایی آروماتیك یا آروماكمیكال ها مولکولهایی هستند كه از محصولات طبیعی به دست میآیند یا به صورت سنتزی ساخته میشوند و بو دارند. بسیاری از مواد شیمایی آروماتیك بوی شبیه مواد طبیعی دارند. به عبارت دیگر شبیه مولکولهایی هستند كه از طبیعت به دست میآیند.
ENFLEURAGE, In this process, aroma materials are absorbed into wax and then the odorous oil is extracted with ethyl alcohol. Extraction by enfleurage was commonly used when distillation was not possible because some fragrant compounds denature through high heat. = انفلوراژ: در این فرایند مواد معطر به داخل یك ماده مومی شكل جذب می شود و سپس روغنهای معطر با اتیل الكل جدا می شود. استخراج با انفلوراژ برای گیاهان ظریف استفاده می شود كه در اثر تقطیر ممكن است ملكولهای مواد معطرشان تخریب شود.
ANIMALIC, Characterized by bodily aromas or aromas most associated with traditional animal materials such as musk, civet and castoreum. These materials are now banned and have been replaced with musks obtained from plants and civet and castoreum smelling molecules obtained synthetically. = انیمالیك یا حیوانی، به بوهایی گفته میشود كه در عطرهای حیوانی سنتی مثل مُشك، سیوت و كاستریوم وجود دارد. این مواد در حال حاضر ممنوع هستند و با مشکهای به دست آمده از گیاهان و مولکولهایی كه بوی شبیه سیوت و كاستریوم میدهند و به صورت سنتزی تشكل شدهاند جایگزین شدهاند.
NEROLI OIL, Neroli essential oil is extracted from the fragrant blossoms of the bitter orange tree and has a beautiful aroma that appeals to men and women alike. In common with rose and jasmine, neroli oil is almost a complete fragrance in itself and forms the heart of one of the worlds most enduring perfumes, ‘Eau de Cologne’. = روغن نرولی: روغنی كه از شكوفه معطر پرتقال تلخ به دست می آید.
AROMATHERAPY, The use of volatile plant oils, including essential oils, for psychological and physical well-being. The therapeutic use of pure essential oils and herbs in body massage,which is described by proponents as “healing, beautifying and soothing” the body and mind.The history of aromatherapy stretches as far back as 6,000 years ago in ancient Egypt. It wasn’t until the 1920’s, however, when the term was actually coined by a French chemist, R.M. Gattefosse. = آروماتراپی، استفاده از روغنهای گیاهی شامل اسانسهای روغنی برای سلامت فیزیكی و فیزیولوژیكی. استفاده درمانی از اسانسهای روغنی خالص و گیاهان در ماساژ بدن، شفابخش، زیباكننده و التیامبخش برای بدن و ذهن میباشد. تاریخچه آروماتراپی به 6 هزار سال پیش به مصر باستان برمیگردد. در سال 1920 این واژه توسط یك شیمیدان فرانسوی به نام گَته فوزه ابداع شد.
aromatherapist
آروماتراپیست
آروماتراپیست
aromatherapy
آروماتراپی، رایحه درمانی
آروماتراپی، رایحه درمانی
fragrance and aroma ingredients
مواد معطر و خوشبو
مواد معطر و خوشبو
8- تبخیر = Evaporation تبخیر
evaporation of sweat = تبخیر عرق
EVAPORATION, The process of changing from a liquid to a vapor. = تبخیر: فرایند تغییر فاز از مایع به بخار
evaporation of sweat = تبخیر عرق
EVAPORATION, The process of changing from a liquid to a vapor. = تبخیر: فرایند تغییر فاز از مایع به بخار
10- قانون = Regulation قانون گذاری
downregulation = کاهش
osmoregulation = تنظیم تراوایی، اسمو رگولاسیون
natural regulation = تنظیم طبیعی
عصب ها دو ضمیمه به نام های آکسون و دندانه دارند.
Seborrhea regulation = تنظیم ترشح چربی توسط غدد چربی
cosmetics regulations = قوانین و مقررات آرایشی بهداشتی
Scalp hyperseborrhea regulation = تنظیم فعالیت بیش از حد غدد چربی پوست سر
functions of the skin are protection, heat regulation, sensation, excretion, secretion and absorption = عملکردهای پوست عبارتند از محافظت، تنظیم دما، لامسه، ترشح چربی و تراوش عرق
downregulation = کاهش
osmoregulation = تنظیم تراوایی، اسمو رگولاسیون
natural regulation = تنظیم طبیعی
عصب ها دو ضمیمه به نام های آکسون و دندانه دارند.
Seborrhea regulation = تنظیم ترشح چربی توسط غدد چربی
cosmetics regulations = قوانین و مقررات آرایشی بهداشتی
Scalp hyperseborrhea regulation = تنظیم فعالیت بیش از حد غدد چربی پوست سر
functions of the skin are protection, heat regulation, sensation, excretion, secretion and absorption = عملکردهای پوست عبارتند از محافظت، تنظیم دما، لامسه، ترشح چربی و تراوش عرق
cosmetics regulations
قوانین و مقررات آرایشی بهداشتی
قوانین و مقررات آرایشی بهداشتی
functions of the skin are protection, heat regulation, sensation, excretion, secretion and absorption
عملکردهای پوست عبارتند از محافظت، تنظیم دما، لامسه، ترشح چربی و تراوش عرق
عملکردهای پوست عبارتند از محافظت، تنظیم دما، لامسه، ترشح چربی و تراوش عرق
regulation
قانون گذاری
قانون گذاری
14- کپسایسین = Capsaicin
15- شیمی آلی = Organic Chemistry شیمی آلی
AROMA CHEMICALS, Molecules obtained from natural products or made by synthetic organic chemistry that have an aroma. Most of the synthetic aroma chemicals are nature identical, i.e., identical to the same molecule obtained from a natural product. = مواد شیمیایی آروماتیك یا آروماكمیكال ها مولکولهایی هستند كه از محصولات طبیعی به دست میآیند یا به صورت سنتزی ساخته میشوند و بو دارند. بسیاری از مواد شیمایی آروماتیك بوی شبیه مواد طبیعی دارند. به عبارت دیگر شبیه مولکولهایی هستند كه از طبیعت به دست میآیند.
شیمی آلی
AROMA CHEMICALS, Molecules obtained from natural products or made by synthetic organic chemistry that have an aroma. Most of the synthetic aroma chemicals are nature identical, i.e., identical to the same molecule obtained from a natural product. = مواد شیمیایی آروماتیك یا آروماكمیكال ها مولکولهایی هستند كه از محصولات طبیعی به دست میآیند یا به صورت سنتزی ساخته میشوند و بو دارند. بسیاری از مواد شیمایی آروماتیك بوی شبیه مواد طبیعی دارند. به عبارت دیگر شبیه مولکولهایی هستند كه از طبیعت به دست میآیند.
شیمی آلی
organic chemistry
شیمی آلی
شیمی آلی
شیمی آلی
شیمی آلی
17- پیوند یونی = Ionic Bonding اتصال از طریق پیوندهای یونی
19- اکسایشی کاهشی = Oxidation Reduction اکسایشی کاهشی
20- پیوندهای شیمیایی = Chemical Bonds پیوندهای شیمیایی
مطلب فوق را در شبکه های اجتماعی زیر با دوستانتان به اشتراک بگذارید