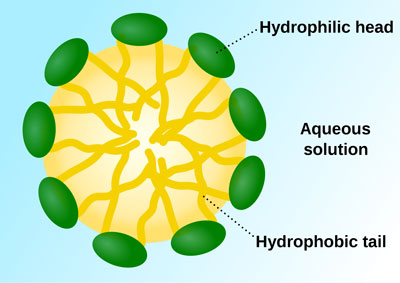
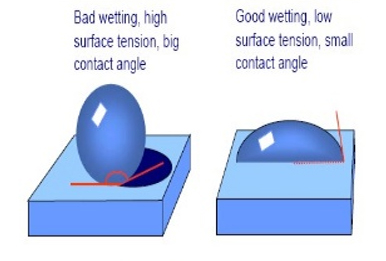
حلالیت = solubility
نویسنده:
چکیده: معادل انگلیسی کلمه یا واژه حلالیت، Solubility می باشد.
حلالیت چیست؟
حلالیت = Solubility
limited solubility = حلالیت محدود
solubility-in-water
واژه «حلالیت» در مقالات سایت احسان حسنانی
فیتواسفینگوزین در محصولات آرایشی بهداشتی
اسفینگوزین یکی از لیپیدهای پوست است. فیتو اسفینگوزینها در واقع اسفینگوزین های گیاهی با خاصیت ضدالتهابی، ضد آکنه و ضدپیری هستند که به عنوان مواد اولیه در صنایع آرایشی بهداشتی کاربرد دارند.
فسفواسفینگوزین یکی از لیپیدهای طبیعی لایه شاخی پوست است. این ترکیب هم به شکل آزاد هم به عنوان بخشی از سرامیدهای پوست، چسبندگی سلول های پوست را ایجاد می کند.
فیتواسفینگوزین ها التیام دهنده، ضدآکنه و ضدپیری هستند و کاربردهای آرایشی بهداشتی گسترده ای دارند. اما به علت مشکلات فرآوری از جمله حلالیت اندک در آب و روغن، بالا بودن دمای انحلال (بالاتر از درجه سانتیگراد)، متبلور شدن در دمای محیط و ریسک تشکیل رسوب با گذشت زمان در فرمولاسیون های آرایشی بهداشتی کمتر استفاده شده است.
مشاهده مطلبسورفکتانت ها: کربوکسیلات ها
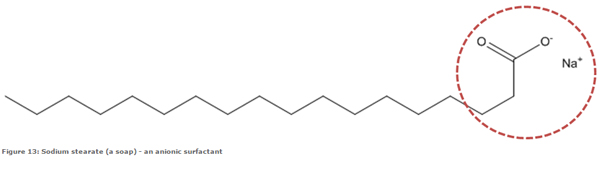
کربوکسیلات ها دسته ای از سورفکتانت های آنیونی هستند که در آن گروه کربوکسیل وجود دارد. صابون ها دسته ای از کربوکسیلات ها می باشند. اتوکسی کربوکسیلات ها، استرکربوکسیلات ها، از دیگر انواع کربوکسیلات ها می باشند.
کربوکسیلات ها دسته ایی از شوینده ها هستند که گروه آبدوست آن ها (گروه آنیونی) از یک گروه کربوکسیل –COOH حاصل شده است. صابون ها نمک های قلیای خاکی اسیدهای چرب می باشند مانند C17H35COONa که نمک سدیمی استئاریک اسید و یک صابون است. هم اکنون کربوکسیلات های اصلاح شده با گروه های عاملی اضافی به صورت تجاری موجود می باشند. این تغییرات موجب افزایش حلالیت در آب های سخت می شود.
مشاهده مطلبسورفکتانت ها: استر کربوکسیلات ها
از واکنش یک الکل چرب با زنجیر بلند با یک اسید چندتایی، استر کربوکسیلات ها به وجود می آیند.مشاهده مطلب
سورفکتانت ها: اتوکسی کربوکسیلات ها
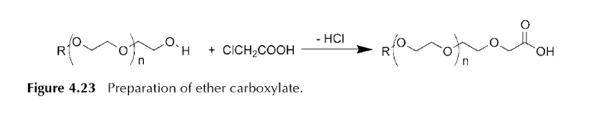
اتوکسی کربوکسیلات ها از واکنش کلرواستیک اسید با اتوکسیلات ها به وجود می آیند.
1- حلالیت:
افزودن گروه اتوکسیله شده موجب افزایش حلالیت محصول در آب می شود. مقادیر HLB از حدود 8 با بهترین حلالیت در حلال های آلی تا 20 یعنی تا اندازه ایی که فقط در حلال های قطبی محلولند، متغیر است. عموماً دیسپرس کننده های خوب صابون آهکی و دارای حلالیت خوبی در محیط های قلیایی هستند.
6- خواص کاربردی:
بهترین خواص شوینده های غیریوی را حفظ می کند. مانند خصلت مرطوب کنندگی بدون واژگونی حلالیت با تغییر دما (بدون نقطه ابری شدن)؛ خواص خوب دیسپرس کنندگی (مثلاً برای پیگمنت ها در رنگ)؛ پایداری خوب کف؛ فعالیت ضد خورندگی خوب؛ بسیار ملایم و بدون الت متراکم شدن روی مو و پوست و همچنین کاهش حساسیت پوست در اثر LES.
مشاهده مطلبسورفکتانت ها: صابون ها
صابون یک سورفکتانت آنیونی از جنس کربوکسیلات است که اسید چرب تشکیل دهنده آن می تواند دودسیل، میریستیل، استئاریک یا اولئیک باشد. مزیت صابون ها آن است که حاوی مواد نفتی نیستند اما عیب بزرگ صابون ها ناپایداری در برابر یون کلسیم و منیزیم (سختی آب) است. صابون پیه، صابون نارگیل، صابون های اولئیک و صابون های تال از انواع مختلف صابون می باشند.
زنجیره های کمتر از C8 محصولاتی با حلالیت بالا در آب تولید می کنند در حالی که بین C8 تا C18 حلالیت کم و بیش از C20 نامحلول در آب می باشند.
پس چرا باید صابون در مقیاس بسیار بزرگی با زداینده های دیگر جایگزین شود؟ عیب بزرگ صابون ها ناپایداری آن ها در برابر یون های فلزات سنگین به خصوص کلسیم و منیزیم بوده که در آب های سخت یافت می شوند و دلیل دیگر، ناپایداری آن ها در برابر اسیدها است. نتیجه نهایی هر دو حالت یکی است، در هر دو حالت صابون از محیط آبی خارج می شود. دلیل این امر حلالیت کم نمک های کلسیمی و منیزیمی اسیدهای چرب و همچنین اسید چرب های آزاد در آب است. این نقطه ضعف موجب رونق تولید مواد فعال سطحی سنتزی شد.
1- حلالیت: صابون C12 اشباع در آب محلولند، صابون های C18 بسیار به آرامی حل می شوند. صابون های C16-C18 غیراشباع در آب محلولند. صابون های پتاسیمی نسبت به انواع سدیمی حلالیت بیشتری دارند (این حالت برای سولفات ها بالعکس است به طوری که انواع پتاسسیمی نامحلول ترند.) نمک های آمین حلالیت بهتری دارند (MEA، DEA، TEA). نمک های TEA (تری اتانول آمین) لوریک اسید و اولئیک اسید نسبت به نوع سدیمی ملایم تر بوده، حلالیتشان بالاتر و کف بهتری دارند اسیدهای چرب روغن تال (ساخته شده با اسیدهای غیراشباع) حلالیت بیشتری در آب داشته و ویسکوزیته کمتری نسبت به انواع حاصل از پیه ایجاد می کنند.
3- سازگاری با یون های آبکی: تمامی نمک های محلول به راحتی به وسیله الکترولیت ها نامحلول شده و عمل Salting out صورت می گیرد. مثلاً به وسیله نمک طعام. صابون ها در آب های سخت خوب عمل نمی کنند (کاهش حلالیت و قدرت کف کنندگی) که علت آن نامحلول بودن نمک های کلسیمی و نمک دیگر فلزات دو یا سه ظرفیتی است.
مشاهده مطلبسورفکتانت ها: دسته بندی شوینده ها
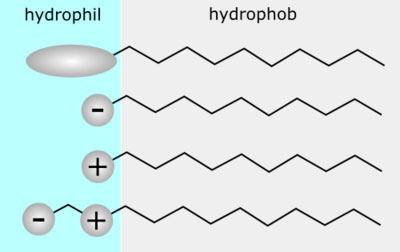
شوینده ها یا سورفکتانت ها را به روش های مختلفی دسته بندی می کنند. بر اساس ساختار شیمیایی، سورفکتانت ها به چهار دسته آنیونی، غیریونی، کاتیونی و آمفوتری طبقه بندی می شوند.
3- اگر گروه آبگریز، یک زنجیره آلکیلی باشد، بهترین خواص شویندگی در محلول آبکی و در محدوده زنجیره های هیدروکربنی C10-C18 خواهد بود. زنجیره های آلکیلی بدون شاخه باعث افزایش ویسکوزیته و دارای خاصیت تجزیه پذیری زیستی بهتر و حلالیت کمتر نسبت به شوینده هایی هستند که زنجیره آن ها به صورت شاخه دار و یا حاوی حلقه است.
4- وجود بیش از یک گروه آبدوست در یک مولکول شوینده موجب افزایش حلالیت و تغییر طول ایده آل قسمت آبگریز به تعداد کربن های بیشتری می شود (طول شاخه آبگریز می تواند از مقدار اپتیمم ذکر شده فراتر رود).
5- اگر مولکول شوینده بتواند با اتیلن اکسید واکنش دهد، میزان حلالیت آن نسبت به مولکول اولیه در آب افزایش می یابد. اتیلن اکسید بیشتر، میزان این حلالیت را افزایش می دهد.
مشاهده مطلبسورفکتانت ها: کف کنندگی شوینده ها
کف از حباب های گاز با دیوارهای نازک از مایع ساخته شده که ساختاری سه بعدی دارد. مایع از دیواره ها به وسیله نیروی گرانش به محل اتصال کشیده می شود. شوینده ها با اثر بر خواص الکترواستاتیکی، ویسکوزیته سطح، ویسکوزیته کل و الاستیسیته فیلم می توانند موجب افزایش میزان کف شوند. روابط بین کف کنندگی و ساختار شیمیایی یک ماده شوینده در این مبحث توضیح داده شده است.
5- افزایش یافتن طول زنیره آبگریز در یک سری همولوگ، باعث افزایش میزان کف تا یک مقدار حداکثر می شود. زنجیره آبگریز بلندتر باعث کاهش بیشتر کشش سطحی و در نتیجه افزایش میزان کف خواهد شد. این امر در شرایطی است که با افزایش طول این زنجیر، حلالیت مولکول مربوطه به سرعت کاهش می یابد.
7- اثر دما بر روی قابلیت کف کنندگی همانند اثر دما بر روی حلالیت مولکول شوینده است. بنابراین شوینده های آنیونی با افزایش دما بیشتر کف می کنند. در حالی که میزان کف کنندگی انواع غیریونی کاهش می یابد.
مشاهده مطلبسورفکتانت ها: ایزوتیونات ها
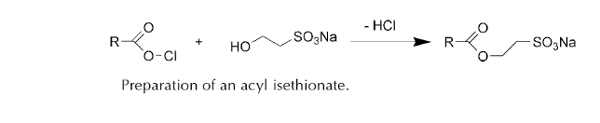
از واکنش اسید کلرید با سدیم ایزوتیونات سورفکتانت های ایزوتیونات ساخته می شوند.
2- حلالیت: نمک سدیمی C12-C14 آن درآب گرم محلول است (محلول %50 در 70oC) ولی در آب سرد حلالیت بسیار کمی دارد (0/01 درصد در 25oC)؛ نمک سدیمی تا %11 در 70oC و %2/5 در 25oC محلول است.
مشاهده مطلبسورفکتانت ها: امولسیون کنندگی شوینده ها
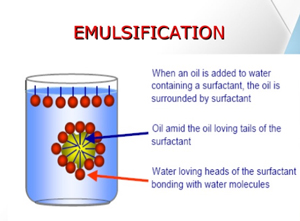
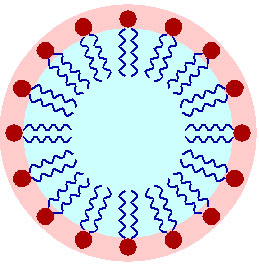
وقتی یک ماده نامحلول مثل روغن به آب حاوی شوینده اضافه می شود، احتمال تشکیل امولسیون وجود دارد. این امولسیون می تواند روغن در آب یا آب در روغن باشد. دو حالت دیگر هم ممکن است به وجود آید که یکی انحلال روغن در آب و یا تشکیل میکروامولسیون ها است. پارامتر HLB ارتباط منطقی بین ساختار شوینده و امولسیون کنندگی آن را نشان می دهد.
حلالیت و امولسیون ها
اگر یک ترکیب نامحلول در آب (مانند روغن های هیدروکربنی) به محلول آبکی شوینده اضافه شود، احتمالات ذیل وجود دارد:
تشکیل امولسیون های روغن در آب (o/w) و آب در روغن (w/o):
شوینده ها بسته به نوع ساختارشان بر روی سطح مابین روغن/آب جذب می شوند (شکل 1-10). هنگامی که شوینده حلالیت زیادتری در فاز یکپارچه داشته باشد، جذب خصلت پایدارکنندگی بسیار حائز اهمیت خواهد بود. این بدان معنی است که در امولسیون های آب در روغن، یک شوینده محلول در آب بسیار کارآمد بوده و در صورتی که امولسیون به صورت روغن در آب باشد، شوینده های محلول در روغن جهت ایجاد امولسیون کارایی بالاتری خواهند داشت.
در عمل مشخص گردیده است که مخلوطی از شوینده ها با حلالیت متفاوت، امولسیون های بهتری از نظر میزان پایداری ایجاد می کنند. بحث پیرامون میکروامولسیون در بخش 1-8-4 دلیل این امر را بیشتر روشن می کند.
عدد
HLB
دما اثر بسیار زیادی بر روی سیستم های امولسیونی ساخته شده با شوینده های غیریونی (اتوکسیله شده) دارد. افزایش دما باعث یک تغییر فاز از o/w به w/o می شود که این جابه جایی به دلیل کاهش حلالیت شوینده های غیریونی در آب در اثر افزایش دما می باشد. دمایی که در ان این تغیر فاز اتفاق می افتد به دمای تغیر فاز (PIT) شهرت یافته است.
حلالیت:
افزایش حلالیت ترکیبات آلی نامحلول در آب، در محلول آبی یک شوینده، در اثر انحلال ترکیب آلی در میسل رخ می دهد. هرچند که ترکیب مذکور در قسمت داخلی میسل است، سطح خارجی میسل، بستگی به ساختار شیمیایی ماده شوینده و ماده آلی دارد. حضور مولکول های هم چیوند با شوینده ها ضروری است، هر چند که بر اساس مشاهدات حدس زده می شود اثرات حلالیت زیر نقطه CMC، در حضور گونه های شبه میسلی صورت می گیرد. این در حالی است که عموماً عمل حل کردن این ترکیبات در بالاتر از نقطه CMC انجام می شود. مقدار حلالیت هیدروکربن هاا و بقیه ترکیبات آلی نامحلول در آب با افزایش اندازه میسل افزایش می یابد. بنابراین گونه های غیریونی حلایت زیادتری نسبت به گونه های یونی ایجاد می کنند. همچنین افزایش طول زنجیره آبگریز شوینده باعث افزایش میزان قدرت حل کنندگی آن مولکول می شود. به وسیله افزودنی هایی با خصلت قطبیت بیشتر (مانند الکل های زنجیره بلند) ظاهر محلول شفافیت کمتری پیدا می کند. استفاده از افزوددنی هایی که از لحاظ شکل و اندازه مشابه مولکول های شوینده باشد، معنی دارتر خواهد بود (بخش 1-8-4 را ببینید).
میکروامولسیون ها:
تشخیص بین امولسیون های ساده و میکروامولسیون ها کار ساده ای است. امولسیون های ساده کلاً ناپایدارند در صورتی که میکروامولسیون ها بی نهایت پایدار هستند. به عبارت دیگر تفاوت بین حل شدن و تشکیل میکروامولسیون به راحتی با یک نگاه ساده قابل تشخیص نیست. در یک دیدگاه جدید میکروامولسیون ها به صورت میسل های متورم شده معرفی شده اند، هرچند که تمامی صاحب نظران با این دیدگاه موافق نبوده و کماکان کشمکش بر سر تفاوت حل شدن و تشکیل میکروامولسیون ها وجود دارد.
شکل
1-11
میزان انباشتگی مولکول ها به اندازه های نسبی گروه های آبگریز و ابدوست بستگی دارد. عامل تأثیرگذار در قسمت آبدوست، اندازه آن می باشد بلکه در صورت یونی بودن، در محلول های شوینده بر روی میزان بار تدثیرگذار است و اگر به صورت زنجیره پلی اتیلن گلیکولی باشد، بر روی میزان حلالیت مؤثر خواهد بود.
در نسبت های تراکمی (P) کمتر از 3/1، توده های کروی در محلول آبکی شکل می گیرند ولی هنگامی که P بین 3/1 و 2/1 باشد میسل هایی استوانه ایی ایجاد می شوند. در P های بین 2/1 تا 1، میکروامولسیون ها به وجود می آیند. اگر P بزرگتر از 1 باشد امولسیون های آب در روغن تولید می شوند (ایجاد میکروامولسیون ها با P بزرگتر از 1) با افزایش Pبه اعداد بزرگتر از 2، امولسیون های درشت با حلالیت کم شکل می گیرند.
این مفهوم نقطه اری شدن را در انواع غیریونی توجیح می کند. افزایش دما اندازۀ مثر سر قطبی را کاهش داده و موجب کاهش حلالیت زنجیره EO می شود. در این حالت P افزایش یافته و موجب ایجاد یک سطح مسطح تر و توده های بزرگتر می شود. همچنین آن ها نامتقارن تر شده و همان طور که انتظار می رود بر روی ویسکوزیته اثر می گذارند. مفاهیم مذکور را می توان برای توجیه ارتباط بین تشکیل میکروامولسیون ها و کشش های سطحی بسیار پایین نیز بسط دارد.
مشاهده مطلبسورفکتانت ها: میسل چیست؟
میسل ها توده های کروی هستند که قسمت درونی آن ها هیدروکربنی است. غلظتی از شوینده که در آن اولین میسل ها تشکیل می شوند، غلظت بحرانی میسل نام دارد. اندازه میسل با کمیتی به نام عدد تجمع اندازه گیری می شود.
1- حلالیت روغن ها و هیدروکربن های آبی در محلول های آبکی.
2- ویسکوزیته
اندازه میسل به وسیله عدد تجمع اندازه گیری می شود که این عدد بیانگر تعداد مولکولهای ماده شوینده شرکت کرده در یک میسل است (جدول 101). چندین نکته جالب توجه در این جدول وجود ارد. اول از همه اینکه بر خلاف انوع آنیونی و کاتیونی، شوینده های غیریونی میسل های بسیار بزرگتری تشکیل می دهند. ممکن است تصور کنید خواصی مانند ویسکوزیته یا حلالیت که به اندازه میسل وابسته است، دلیلی بر وجود این میسل های بزرگ شوینده های غیرینی باشد. در عمل نیز همین طور است زیرا شوینده های غیریونی در حل کردن روغن های هیدروکربنی بسیار کارآمد هستند.
هنگامی که غلظت از این حد افزایش یابد (که بسیاری از شوینده ها نیز در این غلظت های بالا تولید و فروخته می شوند) مثلاً 25 % برای مایعات شوینده فعال و 15 % برای شامپوها، محلول حاصل رفتارهای عجیبی از نظر حلالیت و ویسکوزیته از خود نشان می دهد. علت تغییر شکل میسل ها به دلیل کاهش فضای آزاد برای آن ها است.
2- CMC شوینده های غیریونی و آمفوتری با افزایش الکترولیت به آن ها، چندان تغییر نمی کند. (اثر افزودن ترکیبات آلی بستگی به میزان حلالیت آن ها دارد).
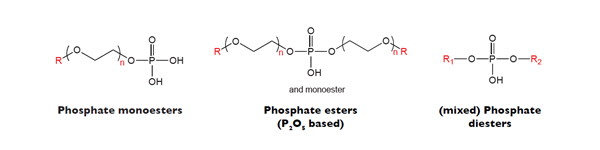
مشاهده مطلبسورفکتانت ها: استرهای فسفات
2- حلالیت: بر اساس قسمت آبگریز، برخی از شوینده های غیریونی فسفاته (در فرم اسیدی) در آب نامحلولند در حالی که نمک های فلزات قلیایی آن ها محلولند هستند. نمک های سدیمی منواسترها با زنجیره های بلند آلکیلی حلالیت ضعیفی در آب دارند. نمک های فلزات قلیایی آن ها محلولند هستند. نمک های سدیمی منواسترها با زنجیره های بلند آلکیلی حلالیت ضعیفی در اب دارند. نمک های فلزات قلیایی محصولات ساخته شده از شوینده های اتوکسیله شده به وسیله واکنش با P2O5 (حاوی مقدار زیادی دی استر) عموماً به طور کامل محلولند. بیشتر محصولات صنعتی، نمک های پتاسیمی هستند که نسبت به نمک های سدیمی حلالیت بهتری دارند.
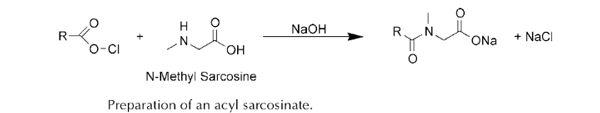
مشاهده مطلبسورفکتانت ها: سارکوزینات ها
2- حلالیت: نمک سدیمی آن چندان در اسید یا pH خنثی محلول نیست ولی کمی در قلیاها قابل انحلال است؛ نمک TEA در pH خنثی حلالیت بیشتری دارد.
مشاهده مطلبسورفکتانت ها: حلالیت شوینده ها
معمولاً حلالیت مولکول های شوینده در آب با افزایش دما افزایش می یابد و معمولاً در دمای خاصی میزان حلالیت به شکل چشمگیری افزایش می یابد که به آن دما نقطه کرافت می گویند. توجه داشته باشیم که برخی شوینده ها از این قانون تبعیت نمی کنند. یعنی با افزایش دما، حلالیتشان کاهش می یابد. کاهش نقطه کرافت باعث افزایش تولید میسل می شود.
حلالیت مولکول های شوینده در محلول های آبکی با افزایش دما زیادتر می شود (به جز استثنائاتی در مورد برخی از شوینده های غیریونی اتوکسیله شده).
شکل 1-6 اثر تغییرات دما بر روی میزان حلالیت سدیم دودسیل سولفات را نشان می دهد.
شکل
1-6
نقطه
Kraft
در یک دمای خاصی میزان حلالیت به صورت چشم گیری افزایش می یابد که این دما به نقطه Kraft مشهور است. این مورد برای کسانی که به طور عملی با مواد شوینده سر و کار دارند بسیار حائز اهمیت است. زیرا امکان ساخت محلول های غلیظ در بالاتر از این نقطه امکان پذیر می باشد. از این رو اگر این دما کمتر از دمای محیط باشد، بسیار مطلب تر خواهد بود. نقطه Kraft دمایی است که بالاتر از تشکیل میسل ها قرار دارد. حلالیت شوینده های غیریونی بر پایه اتیلن اکسید، با افزایش دما کاهش می یابد. نقطه مذکور برای این دسته از شوینده ها یک نقطه تئوری و در دمایی کمتر از صفر درجه می باشد. شوینده های غیریونی اتوکسیله شده ایی که زنجیره آبگریز بزرگی داشته باشند، دارای نقطه Kraft بالاتر از صفر درجه هستند.
نقطه Kraft و حلالیت شوینده های آنیونی به وسیله یون مخالف (کانتریون)، مشخص می گردد. نمک های سدیمی اسیدهای چرب، دارای نقاط Kraft بالاتری نسبت به انواع پتاسیمی آن ها هستند ولی این حالت برای دودسیل سولفات ها بر عکس است. این نقطه در حالتی که نمک کلسیمی اسید چرب با نک سدیمی مقایسه شود، بسیار بالاتر خواهد بود زیرا تمایل انواع کلسیمی جهت ایجاد میسل کمتر از انواع سدیمی است.
بنابراین آبهای سخت (حاوی یون کلسیم) حلالیت صابون ها را کاهش می دهند. به علارت دیگر نمک های کلسیمی اکثر شوینده ها، حلالیت زیادتری در محلول های هیدروکربنی دارد.
1- وارد کردن گروه های اتوکسی به مولکول دودسیل سولفات، باعث افزایش حلالیت می شود (اما افزایش تعداد گروه های EO باعث کاهش CMC نمی شود).
مشاهده مطلبسورفکتانت ها: سولفات ها
جا دارد به این نکته اشاره شود که آلکیل سسولفات های نوع دوم به وسیله واکنش اولئوم با آلفا اولفین های حاصل از مولکول های واکش شکسته شده، تهیه می شوند. این محصولات خواص کلی شوینده های سولفاتی را دارا هستند ولی دارای بوی نامطبوع و رنگ تیره می باشند. به همین دلیل از این ترکیبات دیگر در اروپای غربی استفاده نمی شود. این در حالی است که تولید آن ها نسبتا آسان بوده و با تجهیزات ساده ایی قابل تولید هستند.
خواص گروه سولفات:
1- حلالیت: نمک های فلزات قلیایی حلالیت خوبی در آب دارند.
مشاهده مطلبسورفکتانت ها: الکل سولفات ها
مثال:
سدیم لوریل سولفات ها C12H25SO4Na
تعریف
الکل سولفات ها تنها از الکل های نوع اول خطی که از ترکیبات طبیعی یا به وسیله روش های سنتزی بدست آمده اند، تهیه می شوند. الکل سولفات ها در فرم اسیدی پایدار نبوده، لذا تنها نمک های آن ها به صورت تجاری موجود هستند که متداول ترین نوع، نمک سدیمی آن است. نمک های آمینی بر پایه منو، دی یا تری اتانول آمین و آمونیاک نیز به وسیله بیشتر تولیدکننده ها به بازار عرضه می شود؛ که عموماً اکتیو آن ها بین 30 تا 40 درصد است. محلول های 60-70 درصدی نیز قابل تولید بوده و گاهی توسط تولیدکنندگان تهیه می شوند. الکل سولفات ها امروزه به وسیله عمل سولفاسیون الکل ها با تری اکسید گوگرد تولید می شوند.
خواص عمومی
1- حلالیت: نمک های سدیمی متداول C12-C14 (دودسیل) الکل سولفات، در غلظت بیش از %30 ایجاد ژل می کنند. در زیر %30 در دمای نرمال به صورت مایع هستند ولی با افت دما به زیر 25oC به صورت خمیر نرمی در می آیند (نقطه Kraft، فصل 1). نمک های آمینی (DEA, MEA یا TEA) حلالیت بهتری دارند. DEA حلالیت کمتری نسبت به TEA دارد ولی محلولی با ویسکوزیته کمتر تولید می کند. نمک های آمینی در حین انبارش تیره می شوند بخصوص اگر در معرض نور قرار گرفته باشند. نقطه Kraft به توزیع زنجیره های کربنی در الکل مادر بستگی دارد. یک توزیع وسیع زنجیره کربنی موجب ایجاد نقطه Kraft پایین تری (حدود 10oC) شده و باعث روانی محصول در دمای اتاق می شود. محلول های فتی الکل های سولفاته نقاط ابری شدنی زیر دمای اتاق دارند که این حالت بسته به تولیدکنندگان متفاوت است. دلیل اصلی این تفاوت و مغایرت ها مقدار الکترولیت و الکل آزاد باقیمانده محصول می باشد.
2- شامپوها و مواد آرایشی: دی اتانول آمین لوریل سولفات اغلب جهت بهبود قدرت پاک کنندگی به همراه لورآمینو پروپیونات ها (آمفوتر) استفاده می شود. در گذشته سدیم لوریل سولفات شوینده اصلی شامپو بود ولی حلالیت کمی داشته (به علت وجود ترکیبات معدنی حاصل از پروسه کلروسولفونیک اسید) و جهت ایجاد محلولی شفاف، به آلکانول آمیدها (کوکو منو اتانول آمید با درصد 10-15) یا گلیکول ها نیاز بوده است. اما این ترکیب برای کرم ها و خمیرها بسیار مناسب است.
روش های جدید تولید (با SO3) الکل سولفات هایی با محتوای مواد معدنی کم، الکل کم و در نتیجه با نقطه ابری شدن چایین را امکان پذیر کرده است. برای خمیرها و کرم ها ممکن است افزودن الکل یا نمک جهت ایجاد ناپایداری لازم باشد. گاهی از الکل های C14-C18 برای افزایش ویسکوزیته یا کدورت استفاده می شود. نمک تری اتانول آمین به علت حلالیت بهترف محصولات شفافی ایجاد می کند.
مشاهده مطلبسورفکتانت ها: الکل اتر سولفات ها
خواص عمومی
1- حلالیت: حضور پلی اتیلن اکسید (یک گروه محلول در آب) حلالیت اترسولفات ها را در مقایسه با الکل سولفات ها افزایش داده است. هنگامی که با الکل سولفات ها مخلوط شوند، اتر سولفات ها حلالیت را بهبود می بخشند. بر خلاف آلکیل سولفات ها، اترسولفات ها دارای نقاط ابری و شفاف شدنی در زیر صفر درجه سانتی گراد هستند.
8- خواص کاربردی: شوینده های بسیار خوبی هستند، به طوری که در آب نمک اشباع و آب سخت (بر خلاف AS یا LABS) قدرت شویندگی آن ها کاهش نمی یابد. بنابراین نیازی به مواد کمکی (Builder) مانند پلی فسفات ها نمی باشد؛ میزان شویندگی با افزودن نمک های منیزیم افزایش می یابد؛ خصلت انحلال پذیری خوب، آن ها را برای فرمولاسیون های مایع قلیایی و فسفات دار مناسب ساخته است.
آن ها می توانند حلالیت شوینده های دیگری را که قطبیت کمتری در آب دارند افزایش دهند؛ امولسیفایر بسیار خوب (خصوصاً برای سبوم)؛ عامل ایجاد کف عالی به خصص در حضور الکترولیت ها، ولی میزان کف آن در مقایسه با آلکیل سولفات ها سبک تر است به طوری که در حضور چربی و روغن زودتر باز شده و فرو می نشیندغ در مجموع اتر سولفات ها در حضور سبوم کف پایداری ندارند (بر خلاف آلکیل سولفات ها)، ولی افزودن سارکوزینات ها، بتائین ها یا آلکانول آمیدها می تواند موجب پایداری کف در حضور سبوم شود؛ ادعا می شود که زنجیره آبگریز C12 خواص کف کنندگی بهتری نسبت به C14 ایجاد می کنند (Adam & Neumann 1980)؛ محصولات تولیدشده توسط تولیدکنندگان متفاوت با ترکیب به ظاهر مشابه، ممکن است از لحاظ میزان کف کنندگی به طور محسوسی متفاوت باشند؛ این مورد بیشتر به تفاوت الکل های اتوکسیله شده اولیه مربوط می شود؛ احتمال می رود C10,C9 و C11 به صورت الکل سولفات ها به عنوان عامل فرونشانندۀ کف عمل کنند.
9- عیوب: ناپایداری هیدرولیتیکی.
کاربردها
1- عمومی: در دهۀ 1950 الکل های اتوکسیله شده سولفاته به تدریج در شوینده های دستی ظروف و شامپوها جایگزین الکل سولفات ها شدند. این جایگزینی به دلیل بهبود بخشیدن حلالیت، کف کنندگی، پایداری کف در آب های سخت، ویسکوزدهندگی بهتر به وسیله نمک و کاهش تحریکات چشمی و پوستی بود.
3- شامپوها و مواد آرایشی: شامپوها، شامپو بدن و مایع دستشویی عمده ترین محصولات هستند که از این ترکیب جهت ساخت آن ها استفاده می شود؛ اترسولفاته 2 مول اتوکسیله عموماً در شامپوها برای ایجاد کف حجیم و پایدار (بدون الکانول آمید) استفاده می شود و این در شرایطی است که مقدار سبوم زیاد نباشد؛ اتر سولفات های 3 مول اتوکسیله کف لحظه ایی (ناپایدار) بسیار خوبی دارند که ناپایدارتر و حجیم تر از کف حاصل از نوع 2 اتوکسیله بوده و برای کف های حمام (Foam Bath) مناسب می باشند.
خواص پاک کنندگی و خصلت ویسکوزدهندگی آن با افزایش واحدهای اتیلن اکسید کاهش می یابد. از جهتی دیگر، افزایش اتوکسیلاسیون حساسیت های چشمی و پوستی را کاهش می دهد. محصولاتی با بیش از 12 واحد اتوکسیله ، به عنوان عامل شوینده و کف کننده ملایم و همچنین به عنوان یک عامل سم زدا کاهش دهنه تحریک زایی نیز استفاده می شوند؛ حلالیت آن ها نیز خوب است.
مشاهده مطلبسورفکتانت ها: تئوری شوینده ها
اگرچه مواد شوینده معمولاً با روش های آزمون و خطا فرمول بندی می شوند و با استفاده از تئوری نمی توان بسیاری از مشکلات را حل کرد، اما با این حال برای درک بهتر عملکرد شوینده ها، دانستن تئوری شوینده ها کمک زیادی می کند. پدیده جذب، کشش سطحی، پدیده میسل، خیس کنندگی شوینده، پراکنده سازی، کف کنندگی و امولسیون کنندگی شوینده ها از خواصی هستند که رفتار یک شوینده را توجیه می کنند.
جذب بر روی سطوح است که به مولکول های شوینده، اثراتی همچون کف کنندگی،
مرطوب کنندگی،
امولسیون کنندگی،
پخش کنندگی (دیسپرس کنندگی)
ذرات جامد و شویندگی را می دهد و
خواص میسل است که خواص محلول و توده ایی مولکول های شوینده نظیر ویسکوزیته و حلالیت را ایجاد می کند.
مشاهده مطلبسورفکتانت ها: خیس کنندگی شوینده ها
وقتی قطره آب روی سطحی قرار می گیرد دو حالت پیش می آید: یا روی آن سطح پخش می شود و یا این که شکل قطره محفوظ می ماند. اگر پخش شود، می گوییم سطح خیس شده و اگر شکل قطره محفوظ بماند، آن سطح خیس نشده است. کاهش کشش سطحی آب در اثر افزودن یک ماده شوینده یا سورفکتانت می تواند یک محلول غیرمرطوب کننده را به یک محلول مرطوب کننده تبدیل کند. بین ساختار شیمیایی و مرطوب کنندگی ارتباطاتی وجود دارد که در این قسمت توضیح داده شده است. یکی از عملکردهای ماده شوینده، سوسپانسیون کردن ذرات جامد در یک مایع مثل آب است. به این فرآیند disperse کردن می گویند. تئوری DLVO پایداری سوسپانسیون ها را توجیه می کند.
• افزایش دما، قدرت مرطوب کنندگی را کاهش می دهد. زیرا حلالیت افزایش یافته و جذب را کاهش می دهد. اما این مورد برای انواع غیرقطبی اتوکسیله شده صادق نیست.
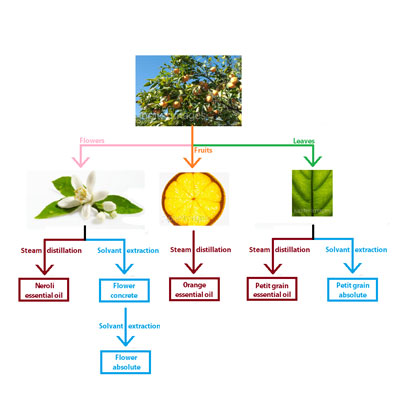
مشاهده مطلبطبقه بندی مواد معطره گیاهان
طبقه بندی محصولات معطر گیاهان را می توان بر اساس مکانیزم جداسازی انجام داد. به محصولات استخراج نام عصاره و به محصولات تقطیر نام اسانس روغنی اطلاق می شود.
- حلالیت (solubility) به محصولات معطر به دست آمده از روش استخراج که با مکانیسم حلالیت جداسازی شده اند نام عمومی « عصاره » اطلاق گردد.
-فراریت (volotility) به محصولات معطر به دست آمده از روش تقطیر که با مکانیسم فراریت جداسازی شده اند نام عمومی «اسانس روغنی» گردد.
مشاهده مطلبمبانی شیمی
حلالیت چیست؟
حلالیت یا انحلال پذیری به بیشترین مقدار ماده ای که در یک دمای معین می تواند در حجم معینی از یک حلال حل شود، گفته می شود.
مشاهده مطلبمحصولات لاغرکننده و ضدچاقی
اگر ماهواره می بینید حتما چپ و راست تبلیغ انواع و اقسام محصولات آرایشی بهداشتی و قرص های لاغر کننده را شنیده و دیده اید.
محصولات لاغری بر پایه کافئین
کافئین معروف ترین و پرکاربردترین ماده تحریک کننده لیپولیز و ماده موثره اصلی اکثر محصولات آرایشی بهداشتی لاغری و آنتی سلولیت است.
استفاده از کافئین در فرمولاسیون های آرایشی بهداشتی مشکل است زیرا کافئین در آب محدودیت حلالیت دارد.
به همین علت محصولات فرموله شده با کافئین معمولاً حاوی الکل می باشند که نکته مثبتی نیست زیرا الکل پوست را خشک می کند.
از الکل برای حل کردن کافئین استفاده می شود.
مشاهده مطلبرنگ مو چیست؟
موهایتان زودتر از آنچه فکر می کردید سفید شده؟ آیا دوست دارید موهایتان را بعد از مدتها رنگ کنید و تنوعی به ظاهرتان بدهید؟ پس این مقاله را حتما بخوانید.
رنگ های موقت یا رنگ موهای قابل آب کشی (color rinses) از اسیدهای با وزن ملکولی بالا یا رنگ های پراکنده شده (dispersed dyes) تهیه می شوند، که تمایل اندکی به مو دارند. می توان این مواد رنگی را با یک پلیمر کاتیونی به صورت کمپلکس درآورد. این کار حلالیت رنگ را کاهش می دهد و در مقابل تمایل جذبی آن به سطح مو را افزایش می دهد. برای پراکنده نمودن آن در پایه رنگ می توان از سورفکتانت استفاده نمود. این کمپلکس مانند روکشی روی سطح مو قرار می گیرد و مازاد آن را می توان پاک نمود. نیروهای پیوستگی بین این مواد با مو ضعیف است و با نخستین بار شستشو از سطح مو پاک می شوند.
این نوع رنگ موها مخلوطی از رنگ های مستقیم می باشند که تا حدود 6 تا 8 بار شامپو زدن، دوام دارند. این نوع رنگ ها معمولاً رنگ هایی با وزن ملکولی پایین می باشند که تنها به لایه های کوتیکول خارجی پوست نفوذ می یابند، بدون آنکه اتصال محکمی با پروتئین های مو برقرار سازند.
رنگ های نیترو (Nitro-dyes) مهم ترین گروه از رنگ هایی هستند که در رنگ موهای نیمه دائمی کاربرد دارند. این رنگ های بدون بار الکتریکی (غیریونی) به سختی تحت تأثیر بارهای منفی سطح مو قرار می گیرند. در نتیجه، با توجه به این امر و همچنین کوچک نمودن جرم ملکولی خود، می توانند به کوتیکول مو نفوذ کنند. شستشوی مو این امکان را فراهم می سازد تا این مواد با توجه به حلالیت در آب، به تدریج از مو خارج شوند. این محصولات حاوی مخلوطی از رنگ های از پیش آماده است که باید برای حدود 30-20 دقیقه بر روی مو قرار گیرد. رنگ حاصل دوام و قدرت عمل بالایی ندارد، زیرا نه فرآیند روشن نمودن رنگ طبیعی مو اتفاق می افتد و نه تأثیری بر موهای خاکستری روی می دهد.
3- رنگ موهای دائمی (Permanent)
این رنگدانه ها نیز همانند رنگدانه های نوع دوم، اندازه کوچکی دارند از این رو به داخل پولک مو نفوذ می کنند. با این تفاوت که با رنگدانه های طبیعی مو ترکیب شیمیایی تشکیل داده در اثر این ترکیب ملکولهای ریز تبدیل به ملکولهای درشت تری می شوند بنابراین در داخل مو محبوس گردیده و لذا اثرشان دائمی است.
مشاهده مطلبمراقبت از پوست کودک و نوزاد
پوست نوزادان و کودکان تفاوت زیادی با پوست نوجوانان و بزرگسالان دارد. پوست نوزاد از پوست فرد بالغ بسیار نازک تر بوده، کمتر شاخی شده، کم موتر است و رطوبت بیشتری دارد. ضخامت پوست، رطوبت پوست، میزان فعالیت غدد سبابه، توانایی پوست نوزاد برای مقابله با عفونت، تفاوت در سیستم ایمنی از جمله این تفاوت ها می باشند. بنابراین به مراقبت های خاصی نیاز دارد و محصولات آرایشی بهداشتی و مراقبت از پوست خاصی را می طلبد.
استفاده از روغن های بچه نیز تأثیر مناسبی در پیشگیری از بروز ادرارسوختگی دارد. این روغن ها معمولاً متشکل از روغن های گیاهی، مشتقات لانولین و الکل ها و استرهای درشت ملکول، می باشند. در بسیاری از محصولات روغن بچه، از پارافین مایع با خلوص زیاد، کمی ماده خوشبوکننده و اندکی افزایش دهنده های حلالیت (solubilizer) نیز استفاده می شود.
محصولات محافظت از پوست نوزاد
از فرآورده های محافظ سنتی برای درمان ادرارسوختگی در کودکان، کرم ها و یا پمادهای حاوی روغن کرچک و زینک اکساید می باشند. زینک اکساید دارای اثرات خفیف ضدعفونی کنندگی، قابض و ضدالتهاب می باشد و در فرآورده های ادرارسوختگی در مقادیر 10-2 درصد به کار می رود.
سایر موادی که در فرآورده های زینک اکساید به منظور اثرات پوشانندگی استفاده می شود شامل وازلین، روغن کرچک، موم زنبور عسل، لانولین، روغن سیلیکون و موم های پلی اتیلنی، می باشند. عصاره های گیاهی نیز در فرآورده های ضد ادرارسوختگی، مورد استفاده قرار می گیرد.
مشاهده مطلبفیلترهای فرابنفش در محصولات آرایشی بهداشتی
فیلترهای فرابنفش ترکیباتی هستند که در محصولات ضدآفتاب استفاده می شوند و از پوست در برابر پرتوهای زیانبار آفتاب محافظت می کنند. فیلترهای فرابنفش به دو دسته فیزیکی و شیمیایی تقسیم بندی می شوند.
فرمول گسترده ومنحنی تضعیف
بنزوفنون-3
بنزوفنون 3 (oxybenzone) علاوه بر جذب اشعه UVB توان جذب اشعه UVA را نیز دارد؛ ولی این ماده بیشتر جهت حفظ کارایی عملکرد ضدآفتابی سایر عوامل جاذب UVB در فرمولاسیون ها به کار می رود. اکسی بنزون یکی از پرکاربردترین مواد محافظ در برابر UVA است و بررسی ها نشان می دهد بین 20 تا 30 درصد از فرآورده های ضدآفتاب موجود در بازار دارای این ماده می باشند. اکسی بنزون به صورت پودر است و حلالیت اندکی دارد. این ماده ممکن است سبب بروز درماتیت های آلرژیک شود، همچنین احتمال بروز سمیت های مزمن سبب شده است تا در فرآورده های کودکان م
ورد استفاده قرار نگیرد.
با توجه به این ویژگی های نامناسب، مشتقات پابا طراحی و سنتز گردید. این مشتقات، حلالیت بهتری در آب دارند و کمتر به داخل لایه شاخی نفوذ می یابند.
استرهای PABA از جمله اکتیل دی متیل پابا
(padimate o)، یکی از پرکاربردترین مشتقات از این گروه می باشند که در مقایسه با پابا اثر لک زایی و تحریک کنندگی کمتر دارد. از دیگر مشتقات در این دسته، آمیل دی متیل پابا و گلیسریل پابا (گلیسریل آمینوبنزوات) می باشد که کاربرد کمتری دارند.
اکتیل متوکسی سینامات
سینامات ها دسته دوم از عوامل شیمیایی ضد UVB می باشند که از نظر FDA، پس از مشتقات PABA بیشترین کاربرد را دارند. اکتیل متوکسی سینامات (octinoxate) قدرت اثر کمتری نسبت به padimate o دارد و در صورت استفاده از فرآورده گاه نیاز است تا برای افزایش کارایی در برابر اشعه UVB از عامل دیگری نیز سود جست. اتوکسی-اتیل پارا – متوکسی سینامات (cinoxate) کاربرد کمتری دارد. ایزوآمیل-پارا-متوکسی سینامات از جمله مشتقاتی است که در اروپا به عنوان ضدآفتاب رسمی شناخته شده است. این مشتقات حلالیت در آب کمی دارند و به راحتی از سطح پوست شسته نمی شوند، به همین منظور کاندیدای مناسبی برای ضدآفتاب های مقاوم به آب و خیلی مقاوم به آب می باشند. حساسیت زایی این مواد زیاد نیست، با این وجود مواردی از حساسیت زایی نوری از کاربرد این فرآورده ها نیز گزارش شده است.
octyl methoxy cinamate
سالیسیلات ها (salicylates)
سالیسیلات ها جاذب های UVB ضعیف تری هستند و معمولاً همراه با سایر عوامل ضدآفتاب فرموله می شوند. از دیدگاه تاریخی این مواد از دیرباز مورد استفاده قرار می گرفته اند ولی با مشتقات کاراتر پابا و سینامات ها جایگزین شدند. از جمله پرکاربردترین مشتقات از این گروه، اتیل هگزیل سالیسیلات (اکتیل سالیسیلات octisalate) و هومومنتیل سالیسیلات (homosalate) می باشند. هر دو ماده فوق توان حل نمودن و همراهی با اکسی بنزون (oxybenzone) و آووبنزون (avobenzone) را دارند. تری اتانول آمین سالیسیلات (trolamine salicylate) از مشتقاتی است که حلالیت آبی بهتری دارد.
مشتقات کامفر
این مشتقات در ایالات متحده به تصویب نرسیده اند، ولی در اروپا شش مشتق کامفر به صورت رسمی در فرآورده ها مصرف می شوند: 4- متیل بنزیلیدن کامفر پرکاربردترین مشتق از این دسته می باشد.
تری آزون ها (triazones)
اکتیل یا اتیل هگزیل تری آزون (EHT) یک جاذب اشعه UVB است که در اروپا پذیرفته شده است (EU no. 15). دی اتیل هگزیل بوتامیدو تری آزون (DBT, Tinosorb M) مشتق جدیدتری است که کارایی بیشتری در جذب اشعه های محدود UVB دارد. بیس – اتیل هگزیل اکسی فنل متوکسی فنیل تری آزون (BEMT, Tinosorb S) مشتق دیگری است که بر طیف وسیعی از اشعه ماورای بنفش و از جمله UVA مؤثر است. بیس اکتیل تری آزول (MBBT) از دیگر مشتقات این گروه با طیف ضدآفتابی وسیع می باشد.
مشاهده مطلبمحصولات معطر گیاهی - آروماتیک های گیاهی
عصاره به محصولات استخراج گفته می شود كه بر اساس مكانیزم «حلالیت» جداسازی گردیده اند.
کنستانتره (Concrete)
کنسانتره محصول استخراج مواد معطر از منابع گیاهی مانند برگها، پوست، گلها و میوههاست که استخراج توسط حلال هیدروکربنی انجام میشود. بعلت حلالیت کم کنسانتره استفاده از آنها محدود میباشد در بیشتر موارد کنسانتره به مقطر تبدیل میشود.
مقطر (Absolute)
بخش قابل حل در الکل از کنستانتره است که توسط استخراج با الکل از کنسانتره بدست میآید. مقطر، مایع و گاهی نیمه جامد است و از آن در عطرسازی استفاده میشود.
رزین ها (Resinoids)
مواد معطری هستند که با استخراج از مواد رزینی گیاه توسط حلالهای هیدروکربنی بدست میآیند.
تنتورها (Tinctures)
محلولهای الکلی هستند که در عطرسازی با خیساندن مواد معطر با الکل آنها را بدست میآورند این مواد میتوانند از منبع حیوانی مانند عنبر و مشک یا از منبع گیاهی مانند صمغها باشند.
مشاهده مطلبتولید محصولات معطر گیاهی
روش های جداسازی محصولات معطر گیاهان بر اساس مكانیزم جداسازی تقسیم بندی می شوند.مشاهده مطلب
آنالیز اسانس های روغنی
آنالیز اسانس های روغنی بسیار مشکل است. زیرا یک اسانس از صدها ترکیب تشکیل شده است.
آنالیز اسانس های روغنی بسیار مشکل است. زیرا یک اسانس از صدها ترکیب تشکیل شده است. کروماتوگرفی گازی معمولا برای جداسازی ترکیبات فرار استفاده می شود. طیف سنجی جرمی، برای تعیین ساختار شیمیایی. مواد قطبیده و غیرقطبیده هر دو می توانند به عنوان فاز مایع ستون کروماتوگرافی استفاده شوند. ایزومرهای نوری در اسانس های روغنی به دو فرم راستگردان و چپ گردان و همچنین مخلوط آنها وجود دارد. روش کروماتوگرافی گازی، روشی بسیار عالی برای ارزیابی ترکیبات تشکیل دهنده اسانس های روغنیست. خروجی ستون کروماتوگرافی، از یک سمت به آشکارساز و از سمت دیگر برای ارزیابی توسط انسان هدایت می شود. به این ترتیب رایحه واقعی اسانس قابل تشخیص و ثبت است.
روشهای کروماتوگرافی
کروماتوگرافی نام عام روشهایی است که بوسیله انها دو یا چند ترکیب در یک مخلوط به طور فیزیکی و بوسیله توزیع متفاوت بین دو فاز از یکدیگر جدا می شوند. این دو فاز عبارتند از یک فاز ساکن که می تواند جامد یا مایع باشد و یک فاز متحرک که گاز یا مایع است و به طور مداوم در فاز ساکن جریان دارد. تفکیک اجزاء مخلوط اساساً نتیجه تمایل متفاوت آنها نسبت به فاز ساکن است. در کروماتوگرافی مایع (LC) فاز متحرک یک مایع است در حالی که در کروماتوگرافی گازی (GC) فاز متحرک یک گاز می باشد. کروماتوگرافی گاز – جامد (GSC) نوعی کروماتوگرافی است که در آن فاز ساکن جامد می باشد. در کروماتوگرافی گاز مایع (GLS)، فاز ساکن مایعی است که بر روی یک تکیه گاه جامد پخش شده است.
کروماتوگرافی اولین بار در سال 1906 بوسیله یک گیاه شناس روسی به نام میشل توت کشف و نامگذاری شد. او سعی داشت رنگدانه های برگهای رنگین را بوسیله عبور دادن محلول عصاره آنها از یک ستون پرشده از ذرات گچ جذب کننده از یکدیگر جدا کند. هر رنگدانه با سرعت متفاوتی به طرف پایین ستون حرکت کرده از یکدیگر جدا شدند. اجزاء جداشده در طول ستون به صورت نوارهای رنگی به آسانی قابل تشخیص بودند. از این رو این روش، کروماتوگرافی به معنای کروما (رنگ) + گرافی (نوشتن) نامگذاری شد.
کروماتوگرافی مایع – مایع (LLC)
این روش در سال توسط مارتین و سینژ ابداع شد. آنها به جای یک ماده جاذب جامد، به عنوان فاز ساکن از مایعی استفاده کردند که روی سطح ماده جامدی پخش شده بود و با فاز مایع متحرک غیرقابل اختلاط بود. اجزاء و ترکیبهای موجود در مخلوط بسته به میزان حلالیت بین این دو فاز پخش می شوند. به خاطر ابداع این روش مارتین و سینژ در سال جایزه نوبل شیمی را دریافت کردند.
کروماتوگرافی کاغذی (PC)
در این روش تفکیک بر روی ورقه های کاغذ صافی صورت می گیرد. پی بردن به مزایای کروماتوگرافی مسطح سبب پیدایش کروماتوگرافی لایه نازک TLC شد. در این روش تفکیک بر روی لایه های نازکی از ماده جاذب پخش شده بر روی صفحات شیشه ای یا صفحات سخت دیگر انجام می شود. روش TLC از زمانی که استال در سال در این زمینه کارهای زیادی انجام داد متداول شد. برای بالا بردن قدرت تفکیک ترکیبهای یونی بوسیله PC یا TLC می توان میدانی الکتریکی در طول کاغذ یا صفحه ایجاد کرد. در این صورت روشهای حاصل به ترتیب الکتروفوز کاغذی و الکتروفوز لایه نازک نامیده می شود.
کروماتوگرافی گازی (GC)
این روش
که اخیراً در بین سایر روشها بیشترین پیشرفت را کرده است ابتدا بوسیله مارتین و جیمز در سال معرفی شد. امروزه این روش پیچیده ترین و متداولترین روش به ویژه برای مخلوط گازها و مایعات و جامدات فرار (مثل روغنهای اسانسی) میباشد. حتی برای مخلوطهای بسیار پیچیده زمان جداسازی بوسیله GC اکنون در حدود چند دقیقه است. قدرت تفکیک بالا، سرعت عمل تجزیه و حساس بودن روش GC سبب شده است که این روش تقریباً در هر آزمایشگاه شیمی متداول و مرسوم باشد.
در مورد کروماتوگرافی گازی بیشتر بدانیم
مشاهده مطلبفرایند عصاره گیری یا استخراج
استخراج به روش جداسازی بر اساس مکانیزم حلالیت گفته می شود. استخراج یکی از مباحث عملیات واحد در مهندسی شیمی است که می تواند جداسازی مایع از مایع یا جداسازی فاز جامد از مایع باشد. در مبحث جداسازی عصاره از گیاهان، استخراج به روش هایی گفته می شود که در آن مواد مؤثره گیاه با مکانیزم حلالیت توسط یک حلال از گیاه جدا می شوند. این حلال می تواند غیر فرار یا فرار باشد. روغن ها و چربی ها از حلال های غیرفرار و گاز بوتان و گاز کربنیک از حلال های فرار به شمار می آیند.
Ref: PHYTOCHEMICAL EXTRACTION, slideshare
استخراج با گازکربنیک
گازکربنیک در فشار زیاد و نقطه بحرانی حلالیت بسیار زیادی دارد که با استفاده از تکنیکهای مناسب و در فشار و دماهای مختلف می توان از این خاصیت برای اسانس گیری استفاده نمود مزیت این روش در مقایسه با سایر روشها آن است که به هیچ وجه باعث تجزیه و هیدرولیز ترکیبات مختلف اسانس روغنی نمی گردد به علاوه بسیاری از ترکیبات که با روشهای دیگر قابل جداسازی نیستند با این روش جداسازی می گردد.
دستگاه استخراج با CO2 طوری طراحی می گردد که بتواند حداکثر تا فشار bar300 و دمای 200 درجه سانتی گراد را تحمل کند(هر چند این کار در دمای 20 درجه و فشار 55 بار انجام می گیرد) گازکربنیک مایع پس از عبور از گیاه و جداسازی اجزاء قابل حل در CO2 وارد ظرفی می شود که باعث تبخیر CO2 گردیده و عصاره را بر جای می گذارد.
با توجه به آنکه گازکربنیک مایع یک حلال لیپوفیل است ترکیبات قطبی در آن نامحلول هستند.
مشاهده مطلباسانس گیری با روش تقطیر
تقطیر یکی از مهمترین روش های جداسازی است که اساس آن بر توزیع اجزاء بین دو فاز است. وقتی مکانیزم جداسازی در فرآیندی فراریت باشد، به آن روش تقطیر گفته می شود. اسانس روغنی گیاهان با مکانیزم فراریت و با روش تقطیر از گیاهان جدا می شود. تقطیر همچنین یکی از مباحث عملیات واحد در مهندسی شیمی است که در آن مواد با دمای جوش متفاوت توسط این فرآیند فیزیکی از هم جداسازی می شوند. تقطیر در فشار محیط، تقطیر با بخار آب، تقطیر در خلأ و تقطیر در فشار روش های مختلف تقطیر می باشند. تقطیر مداوم و تقطیر جزء به جزء نام دو روش مختلف تقطیر در عملیات پالایش نفت می باشند.
اسانس گیری از گیاه با روش تقطیر با بخار آب
در مواردی که تخریب حرارتی گیاه یا هیدرولیز شدن اجزاء استری در آب مسأله است اجزاء معطر این گیاهان با استفاده از مکانیسم حلالیت ( روش شستشو یا استخراج با حلال) جداسازی می گردد.
مشاهده مطلبمعرفی موم زنبور عسل پویان
شرکت پویان بیزواکس اولین تولید کنندهBEESWAX ارگانیک تخصصی در ایران است. موم زنبور عسل این شرکت خالص، بدون افزونی و رنگبرهای شیمیایی می باشد و با روش نانونالیزاسیون تهیه شده است. شرکت پویان بیزواکس در راستای اراده ملی مبتنی بر قطع وابستگی به کشور های خارجی، به حول و قوه خداوند وبا تلاش بی وقفه برای اولین بار در کشور موفق به تولید بیزواکس کاملا ارگانیک و با کیفیت ممتاز و منطبق با استاندارد برای مصارف صنایع ارایشی و بهداشتی گردیده است که در رنگهای ، سفید ، و زرد کم رنگ، ودر شکلهای گرانول و قالبی به صورت عمده و خرده قابل عرضه میباشد.
موم زنبور عسل ظرفیت نگهداری اب پماد ها و کرمها را افزایش میدهد. در صنایع دارویی به عنوان اهسته کننده زیر حلالیت ترکیبات دارویی و لیز کننده قرص ها عمل میکند و براحتی در امولسیونهای اب در روغن و روغن در اب شرکت میکند.
مشاهده مطلبسود پرک چیست؟
سود پرک، با فرمول شیمیایی NaOH، از اصلی ترین مواد شیمیایی صنعتی است و تقریباً همه صنایع بزرگ را پوشش می دهد. سود سوزآور، کاستیک سودا جامد، نام های متداول دیگر این ماده است. شکل ظاهری این ماده به صورت پرک های شیری رنگ جامد دیده می شود و به شدت خاصیت قلیایی دارد. قوی ترین محلول های قلیایی در صنعت با همین سود جامد پرک تهیه می شوند و برای تنظیم PH محلول ها در مراحل مختلف تولید و ... به کار می روند.
• حلالیت در سایر حلال های شیمیایی: محلول در گلیسرول/ حلالیت کم در آمونیاک / نامحلول در اتر / حلالیت آرام در پروپیلن گلایکول
مشاهده مطلبواژه «حلالیت» در منابع و ترجمه های احسان حسنانی

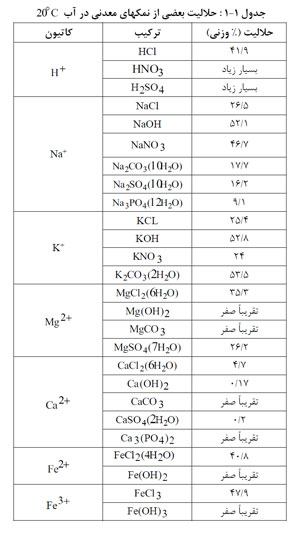
حلالیت برخی از نمک های معدنی در آب
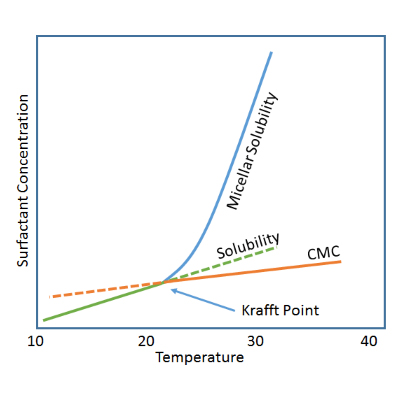
منحنی حلالیت سورفکتانت ها. نقطه کرافت در شکل نمایش داده می شود.

مطلب فوق را در شبکه های اجتماعی زیر با دوستانتان به اشتراک بگذارید